Zum Einstieg
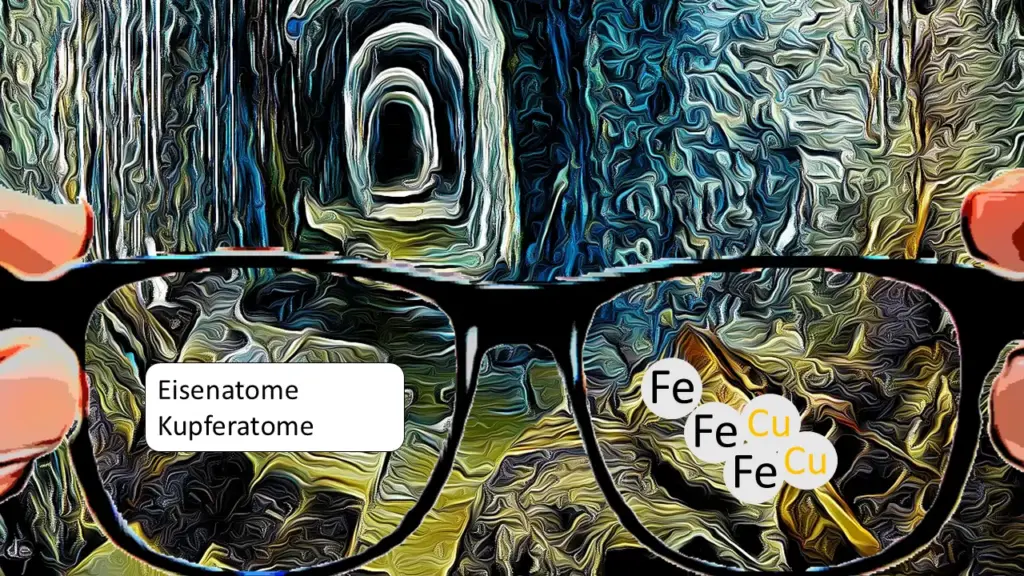
- Beschreibe, was auf dem Foto in Abb. 1 zu sehen ist.
- Stelle mit Hilfe von Galerie 1 Vermutungen auf, welche Stoffe in Abb. 2 abgebildet sind und benenne das Besondere an der Leiter in der Aufnahme.
- Entwickle eine plausible Idee, welcher Stoff möglicherweise außen an der Eisenleiter haften könnte und stelle deine Idee im Plenum vor.
Anregungen zu A3
Prinzipiell könnte die Leiter auch verrosten. Zur Rostbildung werden Wasser, Luftsauerstoff und Eisen benötigt. Dies ist alles vorhanden. Salze im Wasser beschleunigen oftmals zudem den Rostvorgang.
Aber: Die Farbe der Leiter auf dem Bild ist nicht Rostfarben. Untersuchungen können belegen, dass es sich um einen anderen Stoff handelt.
Untersuchungen zeigen, dass die äußere Schicht der Leiter nicht mehr aus Eisen, sondern aus Kupfer besteht.
Begründe, inwiefern die Farben der jeweiligen Stoffe auf das Ergebnis der Untersuchung hindeuten.
Wenn Du magst, versuche schon einen ersten Erklärungsansatz auf Teilchenebene zu finden, wie dort Kupferablagerungen entstanden sein können. Aber das ist etwas, was du heute neu lernen sollst. Also kein Stress!
Ein Kupferbergwerk aus alten Zeiten
Weiteres
Erinnerst du dich daran, dass Menschen wie „Ötzi“ bereits in prähistorischen Zeiten Kupfer herstellen und nutzen konnten? In Europa wurden dafür schon wenig später Kupfererze bis in die Neuzeit hinein aus Bergwerken gefördert.
Röderstollen. Heute UN Weltkulturerbe.1
Im Röderstollen – heute UN Weltkulturerbe – in der Nähe von Goslar wurden zum Beispiel vor über 200 Jahren Kupfersalze unter Tage abgebaut, aus denen man dann reines Kupfer herstellte.
Weiteres
Im Laufe der Zeit hat man das eine oder andere im Stollen liegen gelassen, z.B. eine Eisenleiter, die dort aber nicht einfach nur verrostet ist…
Schau dich um im Röderstollen1
Wirf einmal einen Blick hinein. Und schaue dir die Farben von Kupfer und typischen Kupfersalzen an.
Farbe von Kupfer & Kupferverbindungen
Kupfercarbonat, Kupferchlorid, Kupfersulfat und Kupfer.2
Aufgaben
- Plane einen einfachen Versuch, der unsere Vermutung bezüglich der Abläufe in der Kupfermine stützen oder widerlegen kann. Benenne Chemikalien, die wir verwenden sollten.
- Führe den Versuch nach einer grundlegenden Besprechung durch, protokolliere die Beobachtungen auch in Form von Fotos und werte den Versuch hinsichtlich unserer Vermutung aus.
Anregungen
Die Kupfermine auf Teilchenebene. 3
Kupfersulfat auf Eisen
Materialien
- Pipetten
- Schleifschwämme / Schmirgelpapier
Chemikalien
-
Eisen
- Blech
- Kupfersulfat-Lösung 0,1 mol/L
-
Rotes Blutlaugensalz
- Kaliumhexacyanoferrat(III)-Lösung
Weiteres
Gibt man einige Tropfen Kaliumhexacyanoferrat(III)-Lösung zu einer Lösung, die Eisen(II)-Ionen (Fe2+) enthält, entsteht sofort ein auffällig tiefblauer Niederschlag. Die Reaktion ist eine klassische Nachweisreaktion für Fe2+-Ionen und verläuft sehr empfindlich. Schon geringe Mengen reichen für eine deutlich sichtbare Blaufärbung.
Durchführung
- Das Eisenblech abschmirgeln und dadurch eventuelle Rostflecken entfernen.
- Einen großen Tropfen Kupfersulfat-Lösung auf das Eisenblech tröpfeln.
- Nach einer Weile die Flüssigkeit mit dem weißen Papiertuch aufnehmen.
- Am Rand des Flecks auf dem Papiertuch einen Tropfen der Lösung des rotes Blutlaugensalz geben.
Aufbau.3
Entsorgen und Aufräumen
-
Eventuell noch vorhandene Flüssigkeiten mit einer Pipette aufnehmen und im Sammelbehälter für Schwermetallsalze geben.
-
Alle verunreinigte Labormaterialien spülen.
-
Alle Materialien an ihren Ursprungsort zurückstellen.
Aufgaben
- Begründe, warum der Versuch ein Modellversuch für die in der Höhle ablaufenden Prozesse darstellt.
- Betrachte in M2 die wahrscheinliche ablaufenden Prozesse in der Höhle.
- Formuliere eine abschließende Erklärung für die Beobachtungen. Du kannst sämtliche Bilder und Hilfen nutzen.
Hilfen zur Erklärung
Du kannst dir hier eine gute Animation zu den Abläufen auf Teilchenebene anschauen.
Bedenke: Die Lupe steht in dieser Animation für unsere „Teilchenbrille“. Man kann die Vorgängen nicht derart vergrößern, dass man Teilchen oder Atome sieht. Wie immer werden die Teilchen bzw. Atome hier als runde Kugeln mit einer bestimmten Farbe dargestellt, um sich die Vorgänge besser vorstellen zu können.
Wir haben bereits eine chemische Reaktion kennengelernt, bei der zwischen Atomen Elektronen ausgetauscht wurden: Die Natriumchloridsynthese aus den Elementen.
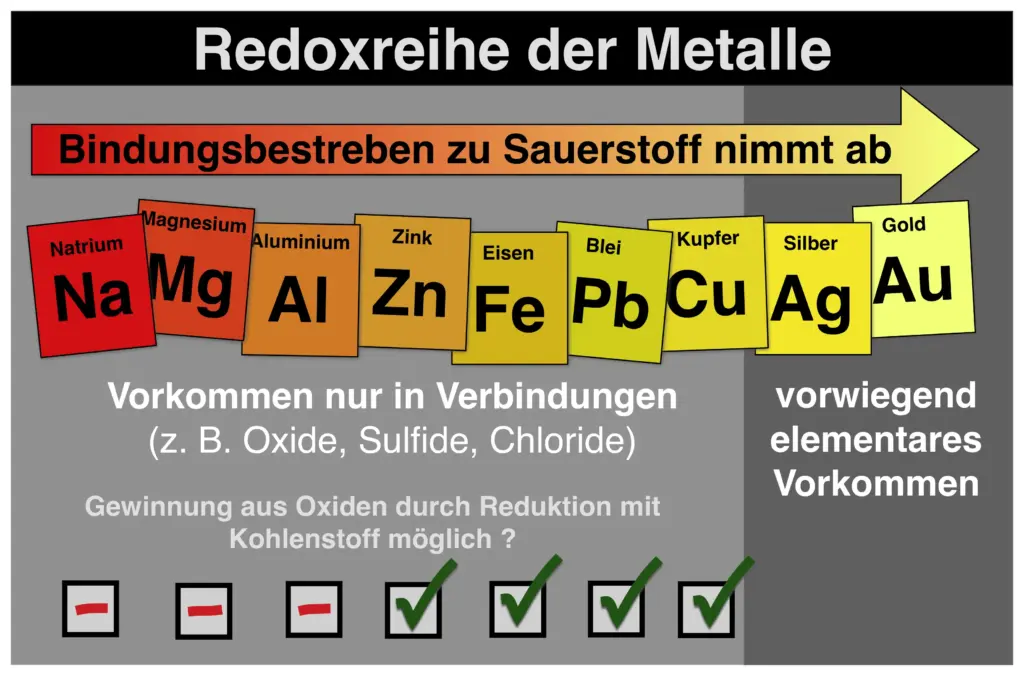
Erinnere dich an die Redoxreihe der Metalle. „Unedlere“ Metalle kommen nur in ihren Verbindungen vor, „edlere“ Metalle gibt es auch elementar auf der Erde.
Atome unedler Metalle geben im Verhältnis einfacher ihre Elektronen ab als die edlerer. Umgekehrt müssten Ionen der edleren Metalle besser Elektronen aufnehmen als Ionen unedlerer Metalle.
Eine Redoxreihe der Metalle.4
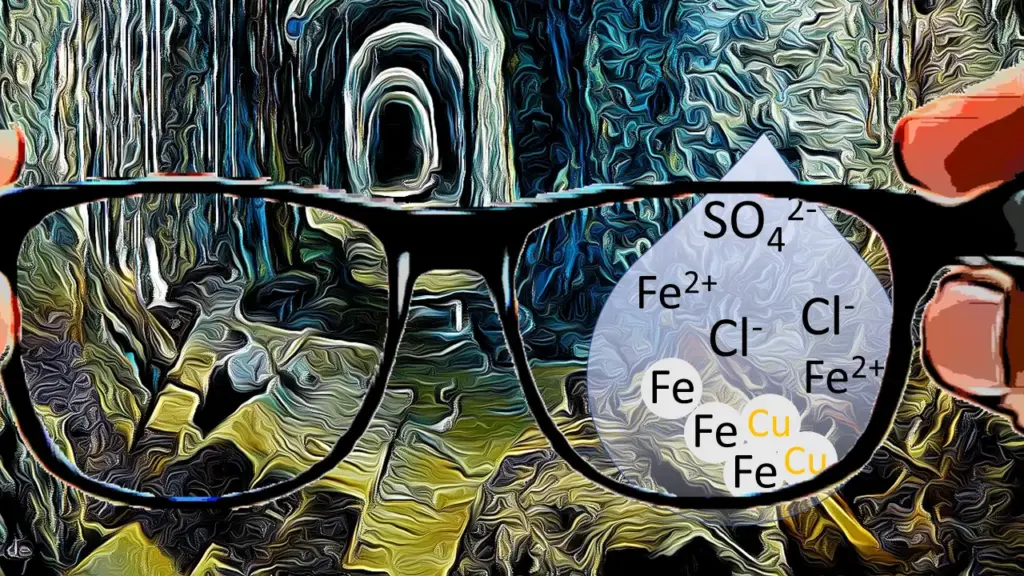
Vor der Reaktion, Eisen-Atome, Kupfer-Ionen
Während der Reaktion, Elektronen, abgeben, aufnehmen,
Kupfer-Atom, Eisen-Ionen, Phasengrenze Metall (Feststoff) – Lösung (Flüssigkeit)
- Wer gibt wem die Elektronen?
- Kupfer-Ionen und Eisenatome reagieren durch „Elektronenübergabe“ zu Kupferatomen und Eisen-Ionen.
- Elektronenübertragungsreaktionen nennt man Redoxreaktionen.
Oxidation und Reduktion5
Ein Wechsel auf Teilchenebene
Was ist hier passiert? Betrachte einmal die folgende nun vollständige Präsentation.
Weiteres
Die Kupfermine auf Teilchenebene.5