Einstieg
Telegrafie ist ein Kunstwort aus den altgriechischen Begriffen für „fern“ und „schreiben“.
Samuel Morse entwickelte hierfür eine Lösung, die binnen weniger Jahrzehnte – beginnend in Amerika – zu einem weltweiten, leistungsfähigen Telegrafie-Netz führte.
Er dachte sich einen Code aus, mit dem man Buchstaben und Zahlen unterscheidbar machte und durch Leitungen schicken konnte.
Elektrische Impulse verbreiten sich zwar mit rasender Geschwindigkeit durch elektrische Leiter, werden aber schwächer, je länger der Leiter wurde. Daher führte er so genannte Relaisstationen ein: Die späteren Telegrafen-Stationen.
Solche Telegrafen-Stationen konnte man in England des 19 Jahrhunderts hervorragend entlang des sich entwickelnden Eisenbahn-Netzes aufbauen. Man benötigte nur eine zuverlässige Spannungsquelle vor Ort!
Weiteres

Portrait von Samuel Morse um 1850 von Matthew Brady 
Künstlerische Darstellung eines Telegrafen (KI generiert) 
Künstlerische Darstellung einer Telegrafen-Station (KI generiert) 
Künstlerische Darstellung eines Schienennetzes mit Telegrafen-Stationen (KI generiert) 
Frühe Daniell-Elemente um 1836 (gemeinfrei) 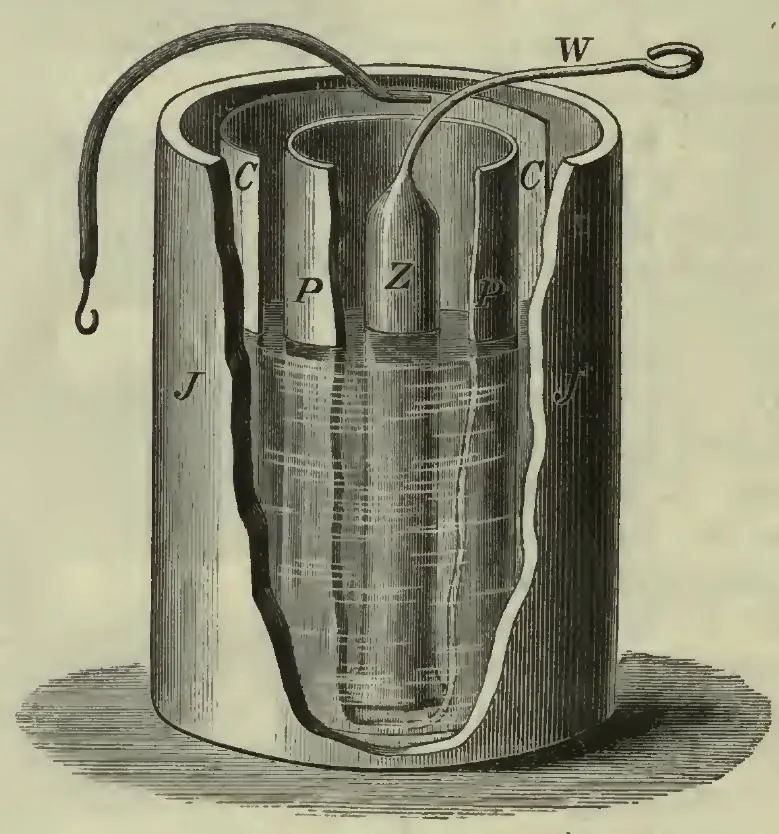
Schnittdarstellung eines Daniell-Elements von William Edward Ayrton (gemeinfrei)
Bilder zum Kontext.
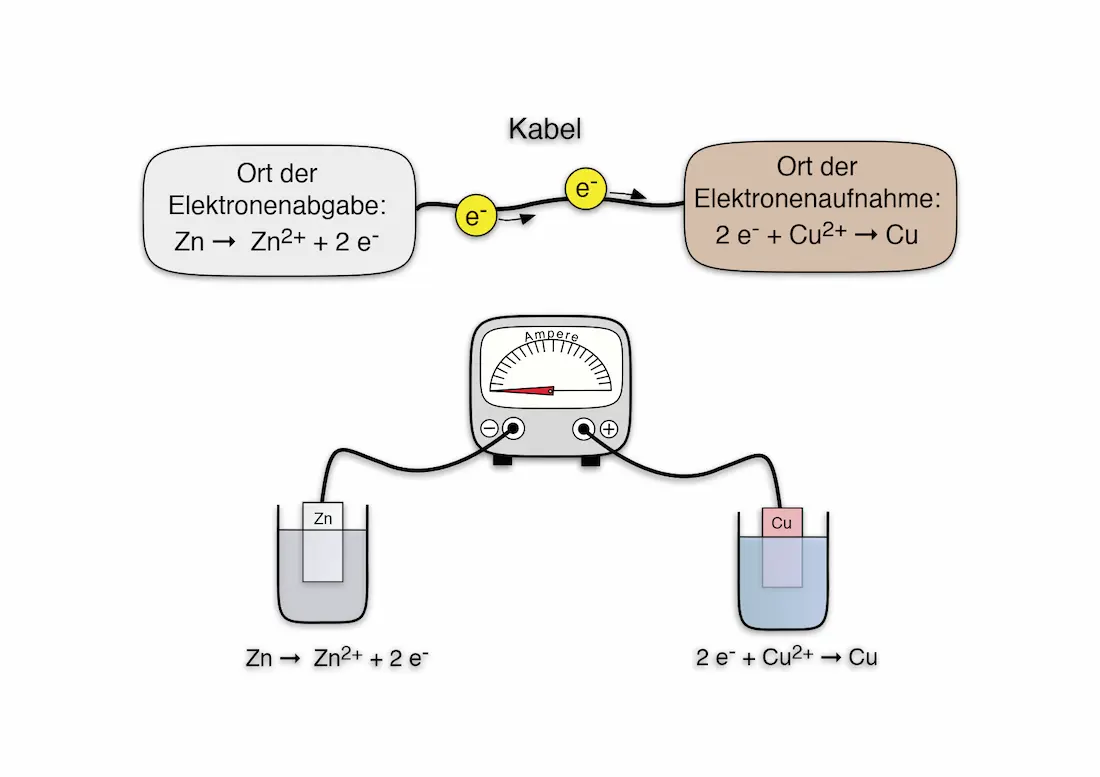
Nachbau eines Daniell-Elements
Materialien
-
Filterpapier
- zugeschnitten & angefeuchtet
- Zellblock
- Spannungsmessgerät
- Multimeter
Chemikalien
- Kupfer-Blech
- Zink-Blech
- Kupfersulfat-Lösung 0,1 mol/L
- Zinksulfat-Lösung 0,1 mol/L
Hinweis
Wir bauen einmal das Daniell-Element nach. Wir stellen die so genannten Halbzellen aber nicht ineinander, sondern der Einfachheit halber nebeneinander. Statt des porösen Steinguts nutzen wir ein Filterpapier.
Durchführung
- Zellblock-Hälften voneinander lösen.
- Filterpapier so zurecht schneiden, dass mit ihm passgenau die beiden seitlichen Löcher/Öffnungen des Zellblockes überdeckt werden können. Ein weiteres Filterpapier mit denselben Maßen zurecht schneiden.
- Filterpapiere doppellagig anfeuchten und zwischen die Zellblock-Hälften legen. Diese wieder zusammenschrauben.
- In eine Halbzelle bis zur inneren Markierung Kupfersulfat-Lösung geben. In die gegenüberliegende Halbzelle Zinksulfat-Lösung bis zur Markierung geben.
- In die Kupfersulfat-Lösung ein abgeschmirgeltes Kupfer-Blech stellen.
- In die Zinksulfat-Lösung ein abgeschmirgeltes Zink-Blech stellen.
- Mit Hilfe eines Multimeters die elektrische Spannung zwischen den beiden Halbzellen in Volt messen.
Entsorgen und Aufräumen
-
Die Flüssigkeiten mit Hilfe der Tropfflaschen aufsaugen. Überschüssige Lösungen in den Entsorgungsbehälter für Schwermetalle geben.
-
Alle verunreinigte Labormaterialien spülen.
-
Alle Materialien an ihren Ursprungsort zurückstellen.
Was wäre wenn ...?
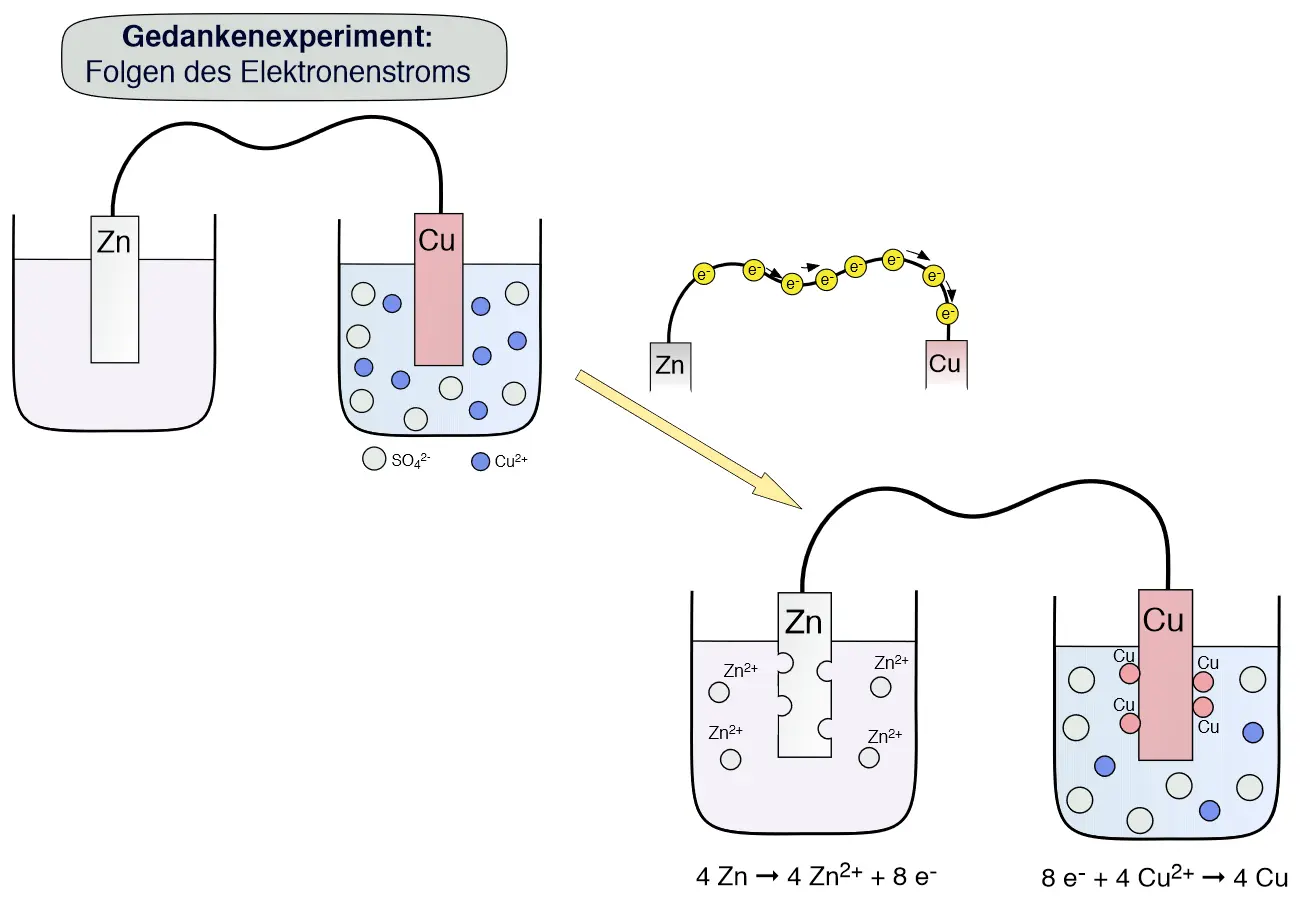
Gedankenexperiment 1
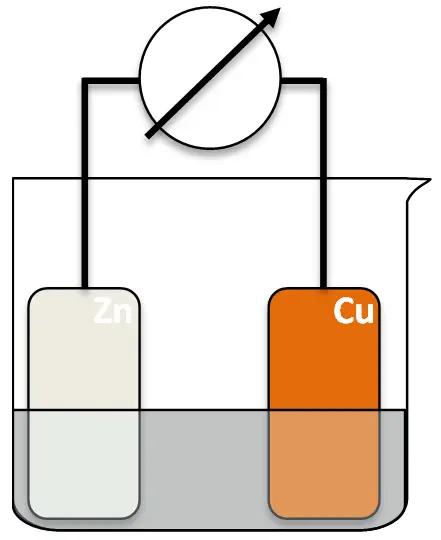
Was würde passieren, wenn man die beiden unterschiedlichen Metall-Bleche lediglich in ein Becherglas mit Wasser stellt?
Gedankenexperiment 1.1
Gedankenexperiment 2
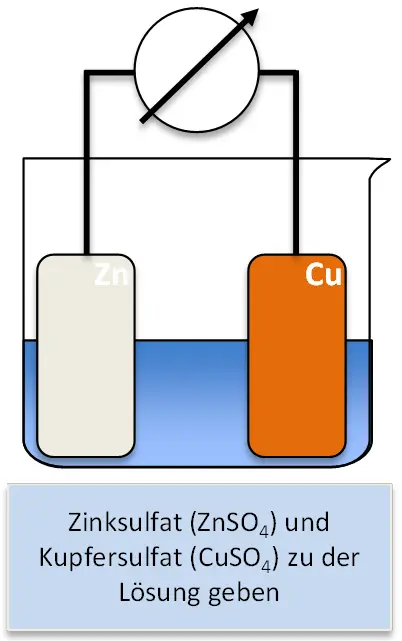
Was würde passieren, wenn man beide Metallsalz-Lösungen einfach in ein Becherglas geben würde?
Gedankenexperiment 2.1
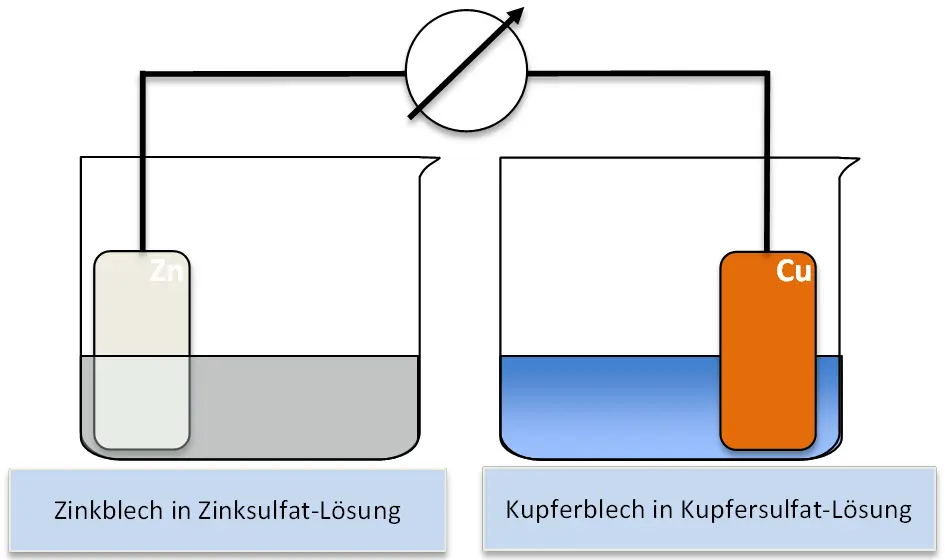
Gedankenexperiment 3
Warum reicht es nicht, die Orte der Oxidation und Reduktion einfach voneinander zu trennen?
Gedankenexperiment 3.2