Man müsste doch bei bekannter Säurekonzentration und Säurestärke einen zu erwartenden pH-Wert der sauren Lösung berechnen bzw. voraussagen können, oder?
Aufgaben
- Vollziehen Sie die Herleitungen der Formeln zur Berechnung von pH-Werten in M1 M2 und M3 nach.
- Bei einer sauren Lösung wird ein pH-Wert von 4 gemessen. Erläutern Sie, dass es anhand dieses Messwertes nicht möglich ist, zu entscheiden, ob eine starke oder schwache Säure vorliegt.
pH-Werte berechnen bei Lösungen von starken Säuren und Basen
Die Säure hat die Stärke, die Lösung den pH-Wert!
Weiteres
Starke Säuren und Basen haben sehr kleine pKS– bzw. pKB-Werte. Die Moleküle oder Ionen liegen in wässriger Lösung nahezu vollständig dissoziiert vor. Es stellt sich in wässriger Lösung jeweils ein Protolysegleichgewicht ein, welches nahezu vollständig auf der Produktseite liegt. Daher kann vereinfachend die Oxoniumionen-Konzentration im dynamischen Gleichgewicht mit der Anfangskonzentration c0 der Säure gleichgesetzt werden. Der pH-Wert bzw. pOH-Wert lässt sich dann wie folgt berechnen:
pH-Werte berechnen bei Lösungen von weniger starken Säuren und Basen
Weiteres
Die Moleküle oder Ionen weniger starker Säuren und Basen dissoziieren hingegen nicht vollständig, sondern nur in geringeren Anteilen. Es stellt sich in wässriger Lösung ein Protolysegleichgewicht ein, welches, ungleich bei starken Säuren oder Basen, nicht nahezu vollständig auf der Produktseite liegt! Der pH-Wert lässt sich dennoch berechnen, wenn die Säure- bzw. Basenkonstante KS / KB und die jeweilige Ausgangskonzentration c0 der Säure bzw. Base bekannt sind:
Für weniger starke Säuren
Für weniger starke Basen
Die hier hergeleiteten Formeln kann man immer verwenden, wenn es darum geht, den pH-Wert von Lösungen mit Säuren und Basen zu berechnen. Es ist gut, wenn Du ihre Herleitung kennst, sie auswendig lernen musst Du aber nicht!
pH-Werte berechnen bei Lösungen von schwachen Säuren und Basen
Weiteres
Die Moleküle oder Ionen schwacher Säuren und Basen dissoziieren hingegen kaum. Es stellt sich in wässriger Lösung ein Protolysegleichgewicht ein, welches, nahezu vollständig auf der Eduktseite liegt! Für schwache Säuren und Basen kann man daher die folgende Annahme treffen:
Mit dieser Annahme lässt sich die Berechnung des pH-Wertes wie folgt vereinfachen. Eine p-q-Formel ist dann nicht mehr von Nöten:
Für weniger starke Säuren
Für weniger starke Basen
Bei den Formel 13 und Formel 18 wird das dritte und vierte Logarithmusgesetz kombiniert angewandt:
Mehr Informationen zu den vier Logarithmusgesetzen findest du hier.
Übung
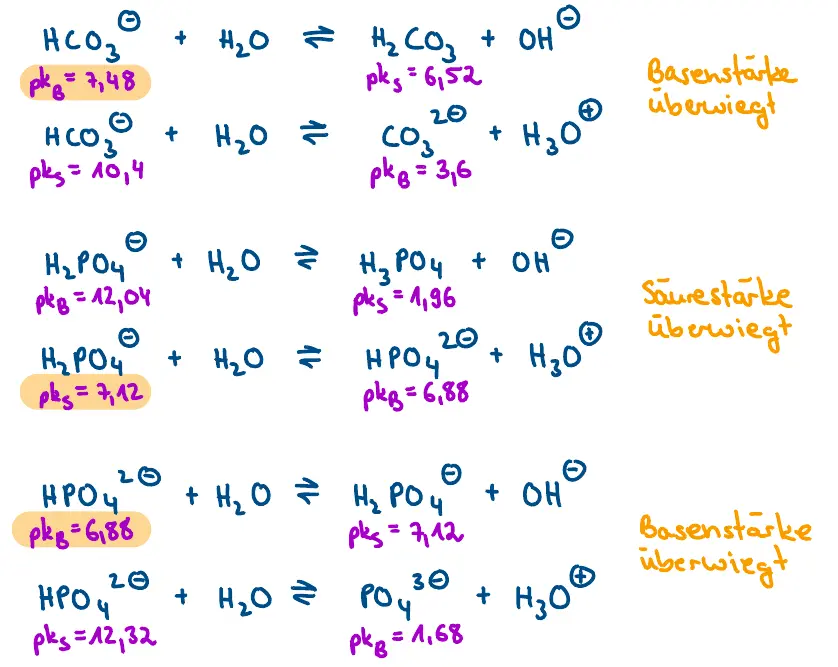
- Stellen Sie die Protolysegleichgewichtsreaktionen der folgenden Stoffe mit Wasser auf. Geben Sie an, ob jeweils die Säure- bzw. Basenstärke überwiegt. Berechnen Sie den pKS– bzw. pKB-Wert der korrespondierenden Säure bzw. Base.
- HCO3– (pKS = 10,4 / pKB = 7,48)
- H2PO4– (pKS = 7,12 / pKB = 12,04)
- HPO42- (pKS = 12,32 / pKB = 6,88)
- Geben Sie die Protolysegleichgewichtsreaktion mit Wasser an und berechnen Sie den pH-Wert der Lösungen mit Hilfe der finalen Formeln aus M1, M2 und M3. Nutzen Sie hierfür auch Material M2 aus der vorherigen Seite!
- Blausäure, c0(HCN) = 0,5 mol/L
- Natriumacetat, c0(CH3COONa) = 1,2 mol/L
- Ammoniumchlorid, c0(NH4Cl) = 0,3 mol/L
- Natriumchlorid, c0(NaCl) = 1 mol/L
- Natriumsulfid, c0(Na2S) = 1,5 mol/L
- Benennen Sie eine Auffälligkeit in den berechneten pH-Werten je Stoff in Aufgabe 4 unter der Verwendung unterschiedlicher Formeln und ziehen Sie ein begründetes Fazit.
Lösungen

Auffälligkeiten
- Die pH-Werte unterscheiden sich deutlich von Formel M1 zu Formel M2 / M3. Eine Ausnahme stellt Natriumsulfid dar.
- Die pH-Werte mittels den Formeln M2 und M3 unterscheiden sich nie oder marginal bei Natriumsulfid.
- Bei Natriumchlorid wäre ein basischer pH-Wert erwartbar gewesen, der pH-Wert suggeriert jedoch eine saure Lösung.
Für starke Säuren und Basen liefert die Formel in M1 ein annehmbares Ergebnis für den pH-Wert. Für schwache Säuren und Basen liefern sowohl Formel M2 und M3 scheinbar das gleiche Ergebnis. Die Formel in M1 weicht zu sehr vom „Realzustand“ ab. Es schließt sich die Frage an, ob die Formel in M3 unter bestimmten Szenarien ein anderes Ergebnis liefert als die Formel in M2.
