Der Ammoniak-Ammonium-Puffer
- In ein Becherglas werden 50 mL Ammoniak der Konzentration c(NH3) = 1,5 mol/L gegeben. Welchen pH-Wert hat die Lösung? Kontrolle: pH = 9,42
- Wieviel Gramm Ammoniumchlorid (NH4Cl) müssen hinzugegeben werden, damit die Pufferkapazität maximal wird? (M(NH4Cl) = 53,5 g/mol) Kontrolle: 4,01 g
- Zum hergestellten Ammoniak-Ammonium-Puffer aus A2 werden 5 mL Salzsäure der Konzentration c(HCl) = 2 mol/L zugegeben. Welchen pH-Wert nimmt die Lösung ein? Wie lautet die Reaktionsgleichung? Kontrolle: 9,12
- Zum hergestellten Ammoniak-Puffer aus A2 werden 25 mL Salzsäure der Konzentration c(HCl) = 4 mol/L zugegeben. Welchen pH-Wert nimmt die Lösung ein? Kontrolle: 0,52
- Zum hergestellten Ammoniak-Ammonium-Puffer aus A2 werden 5 mL Natronlauge der Konzentration c(NaOH) = 3 mol/L zugegeben. Welchen pH-Wert nimmt die Lösung ein? Wie lautet die Reaktionsgleichung? Kontrolle: 9,42
- Wie viel mL Salzsäure oder Natronlauge der Konzentration 2 mol/L müsste man zur Pufferlösung aus A2 hinzugeben, damit die Pufferkapazität erschöpft ist? Kontrolle: 30,5 mL
- Ein anderer Ammoniak-Ammonium-Puffer hat einen pH-Wert von 8,5. Wie groß ist das prozentuale Verhältnis der Konzentration von Ammoniak zu Ammonium in dieser Pufferlösung? Welche Ammoniak-Konzentration liegt vor, wenn die Konzentration der Ammonium-Ionen bei 0,2 mol/L liegt? Kontrolle: 85 % NH4+ und 15 % NH3
- Es werden 200 mL Salzsäure der Konzentration 0,1 mol/L, 600 mL Ammoniumchlorid-Lösung der Konzentration 0,1 mol/L und 200 mL Ammoniak-Lösung der Konzentration 0,2 mol/L zusammengegeben. Welchen pH-Wert hat die Lösung? Kontrolle: 8,64
- Mit welchen Herausforderungen sehen Sie sich konfrontiert, den pH-Wert der Lösung rechnerisch zu ermitteln, wenn zum hergestellten Puffer aus A2 eine schwache Säure (z.B. Essigsäure) hinzugegeben wird?
Anregungen & Lösungen
- Entscheide anhand des pKB-Wertes von Ammoniak, welche Formel zur pH-Wert-Berechnung du hier sinnvollerweise nutzen solltest.
- Die Pufferkapazität ist maximal, wenn in der Pufferlösung die gleichen Anteile an Puffer-Säure und korrespondierender Puffer-Base enthalten ist.
- Berechne zunächst die Stoffmenge an Ammoniak der Lösung aus A1. Dieselbe Stoffmenge an Ammoniumchlorid muss zugegeben werden.
- Rechne die Stoffmenge von Ammoniumchlorid in eine Masse in Gramm um.
- Berechne zunächst, welche Stoffmenge an Oxonium-Ionen zum Puffer hinzugegeben werden.
- Wende die Henderson-Hasselbalch-Gleichung an und passe den Quotienten entsprechend der zugegebenen Stoffmenge an Oxonium-Ionen an.
- Berechne zunächst, welche Stoffmenge an Oxonium-Ionen zum Puffer hinzu gegeben werden.
- Vergleiche dann die Stoffmenge mit der Stoffmenge an Puffer-Base im Puffersystem: Was fällt dir auf?
- Ausgehend von deinen Auffälligkeiten: Überlege wie der pH-Wert nun berechnet werden kann.
- Berechne zunächst, welche Stoffmenge an Hydroxid-Teilchen zum Puffer hinzu gegeben werden.
- Wende die Henderson-Hasselbalch-Gleichung an und passe den Quotienten entsprechend der zugegebenen Stoffmenge an Hydroxid-Ionen an.
- Bei Zugabe von Salzsäure verringert sich der pH-Wert. Die Pufferkapazität ist i.d.R. dann erschöpft, wenn sich der pH-Wert durch die Säure-Zugabe um 1 verringert hat, ausgehend vom pKS-Wert: pH = pKS – 1.
- Betrachte die Henderson-Hasselbalch-Gleichung: Wenn der Logarithmus vom Quotient 1 ergibt, wäre die zuvor getroffene Annahme erfüllt. D.h. wann gilt: lg x = 1 ? Wenn x = 10!
- Setze den Quotienten der Henderson-Hasselbalch-Gleichung also mit 10 gleich und löse zur Stoffmenge der hinzugegebenen Oxonium-Ionen auf.
- Setze den pH-Wert in die Henderson-Hasselbalch-Gleichung ein und löse zum Quotient der Stoffmengen der Pufferkomponenten auf.
- Rechne das Ergebnis in Prozent um.
- Es handelt sich hierbei um eine Ammoniak-Ammonium-Pufferlösung, zu der formal Salzsäure gegeben wird.
- Berechne zunächst die Stoffmengen der Pufferkomponenten und der mit der Salzsäure hinzugegebenen Oxonium-Ionen aus und verfahre dann wie in A3.

Hier liegt ein Fehler vor: Der pOH-Wert beträgt nicht 4,58, sondern 2,29. Folglich liegt der pH-Wert nicht bei 9,42, sondern bei 11,71.
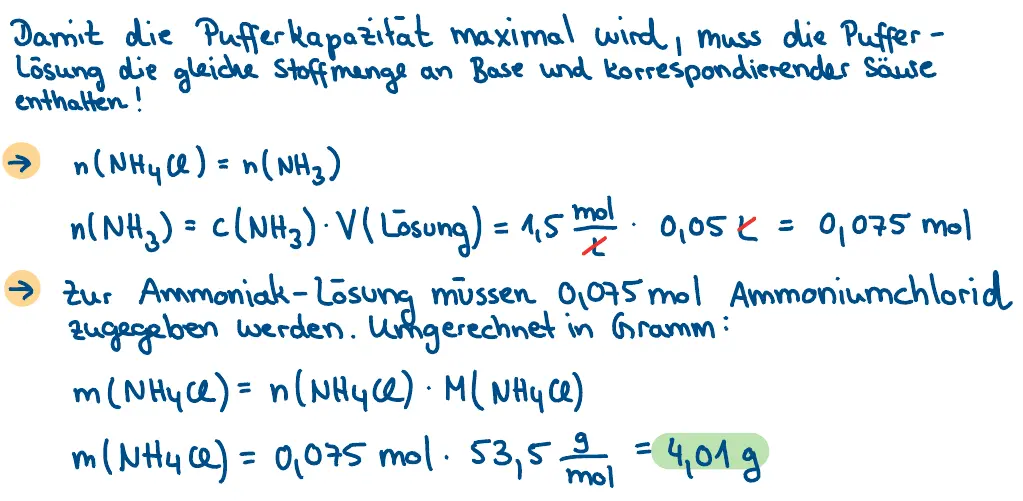

- Wir berechnen zunächst die Stoffmenge an zugeführten Oxonium-Ionen.
- Aus A2 wissen wir bereits, dass 0,075 mol Pufferbase enthalten sind.
- Ein Vergleich der Stoffmengen lässt erkennen: Die Stoffmenge an Pufferbase reicht nicht aus, um die zugeführte Stoffmenge an Oxonium-Ionen abzupuffern. Folglich wird der Puffer hier komplett aufgebraucht.
- Die übrig gebliebenen Oxonium-Ionen bestimmen nun maßgeblich den pH-Wert der Lösung. Er lässt sich über die klassische Formel für starke Säuren berechnen
Berechnung Stoffmenge Oxonium-Ionen
Berechnung übrig gebliebener Stoffmenge an Oxonium-Ionen nach der Pufferung
Berechnung der Konzentration an Oxonium-Ionen in der Lösung
pH-Wert-Berechnung







- Wenn eine schwache Säure, zum Beispiel Essigsäure, zu unserem Ammonium-Ammoniak-Puffer hinzu gegeben wird, reagiert die zugesetzte Säure mit dem Ammoniak, wodurch Acetat-Ionen gebildet werden, die die korrespondierende Base zur Essigsäure bilden.
- Folglich entsteht in unserer Lösung ein zweites Puffersystem: Der Essigsäure-Acetat-Puffer.
- Beide Puffersysteme bedingen den pH-Wert der Lösung gemeinsam. Grundlage hierfür ist ein gemeinsamer Gleichgewichtszustand, der durch eine einzige Henderson-Hasselbalch-Gleichung nicht abgebildet werden kann.
- Die pH-Wert-Berechnung wird erheblich komplizierter. Für diesen Fall fehlt uns das notwendige Handwerkszeug.
Der Dihydrogenphosphat-Hydrogenphosphat-Puffer
- In ein Becherglas werden 80 mL Natriumdihydrogenphosphat der Konzentration c(NaH2PO4) = 2 mol/L gegeben. Welchen pH Wert hat die Lösung? Kontrolle: pH = 3,41
- Wieviel Gramm Dinatriumhydrogenphosphat (Na2HPO4) müssen hinzugegeben werden, damit die Pufferkapazität maximal wird? M(Na2HPO4)=142 g/mol – Kontrolle: m(Na2HPO4) = 22,72 g
- Zum hergestellten Dihydrogenphosphat-Hydrogenphosphat-Puffer aus A9 werden 5 mL Salzsäure der Konzentration c(HCl) = 1,5 mol/L zugegeben. Welchen pH-Wert nimmt die Lösung ein? Wie lautet die Reaktionsgleichung? Kontrolle: pH = 7,08
- Zum hergestellten Dihydrogenphosphat-Hydrogenphosphat-Puffer aus A9 werden 5 mL Natronlauge der Konzentration c(NaOH) = 2 mol/L zugegeben. Welchen pH-Wert nimmt die Lösung ein? Wie lautet die Reaktionsgleichung?
Kontrolle: pH = 7,16 - Wie viel mL Salzsäure oder Natronlauge der Konzentration 3 mol/L müsste man zur Pufferlösung aus A9 hinzugeben, damit die Pufferkapazität erschöpft ist?
Kontrolle: V(HCl) = V(NaOH) = 43,63 mL - Ein anderer Dihydrogenphosphat-Hydrogenphosphat-Puffer hat einen pH-Wert von 6. Wie groß ist das prozentuale Verhältnis der Konzentration von Dihydrogenphosphat zu Hydrogenphosphat in dieser Pufferlösung? Welche Hydrogenphosphat-Konzentration liegt vor, wenn die Konzentration der Dihydrogenphosphat-Ionen bei 0,2 mol/L liegt? Kontrolle: n(HPO42-) : n(H2PO4–) = 7,1 % : 92,9 % und c(HPO42-) = 0,0152 mol/L
- Es werden 100 mL Salzsäure der Konzentration 0,1 mol/L, 400 mL Dihydrogenphosphat-Lösung der Konzentration 0,2 mol/L und 300 mL Hydrogenphosphat-Lösung der Konzentration 0,3 mol/L zusammengegeben. Welchen pH-Wert hat die Lösung? Kontrolle: pH = 7,17
- Ein Liter eines Dihydrogenphosphat-Hydrogenphosphat-Puffers, das 0,1 mol der jeweiligen Stoffkomponenten enthält, soll durch Zugabe von Salzsäure auf einen pH-Wert von 7 eingestellt werden. Wieviel mL Salzsäure der Konzentration 2 mol/L sind hierzu nötig? (Die Volumenänderung soll hierbei unberücksichtigt bleiben.) Kontrolle: V(HCl) = 6,85 mL
- Schlagen Sie ein Puffersystem vor, mit dem man bei einem pH-Wert von 6 puffern kann. Berechnen Sie das genaue Verhältnis zwischen der Säure und der korrespondierenden Base.
- Ein Schüler schlägt ein Puffersystem bestehend aus Hydrogenphosphat- und Phosphat-Ionen vor, um eine Lösung bei einem pH-Wert von 12 zu puffern. Erklären Sie dem Schüler, dass sein Vorschlag keine gute Idee ist.
Anregungen
- Entscheide anhand des pKS-Wertes von Dihydrogenphosphat, welche Formel zur pH-Wert-Berechnung du hier sinnvollerweise nutzen solltest.
- Die Pufferkapazität ist maximal, wenn in der Pufferlösung die gleichen Anteile an Puffer-Säure und korrespondierender Puffer-Base enthalten ist.
- Berechne zunächst die Stoffmenge an Natriumdihydrogenphosphat in der Lösung aus A8. Dieselbe Stoffmenge an Dinatriumhydrogenphosphat muss zugegeben werden.
- Rechne die Stoffmenge von
- Dinatriumhydrogenphosphat in eine Masse in Gramm um.
- Berechne zunächst, welche Stoffmenge an Oxonium-Ionen zum Puffer hinzugegeben werden.
- Wende die Henderson-Hasselbalch-Gleichung an und passe den Quotienten entsprechend der zugegebenen Stoffmenge an Oxonium-Ionen an.
- Berechne zunächst, welche Stoffmenge an Hydroxid-Teilchen zum Puffer hinzu gegeben werden.
- Wende die Henderson-Hasselbalch-Gleichung an und passe den Quotienten entsprechend der zugegebenen Stoffmenge an Hydroxid-Ionen an.
- Bei Zugabe von Salzsäure verringert sich der pH-Wert. Die Pufferkapazität ist i.d.R. dann erschöpft, wenn sich der pH-Wert durch die Säure-Zugabe um 1 verringert hat, ausgehend vom pKS-Wert: pH = pKS – 1.
- Betrachte die Henderson-Hasselbalch-Gleichung: Wenn der Logarithmus vom Quotient 1 ergibt, wäre die zuvor getroffene Annahme erfüllt. D.h. wann gilt: lg x = 1 ? Wenn x = 10!
- Setze den Quotienten der Henderson-Hasselbalch-Gleichung also mit 10 gleich und löse zur Stoffmenge der hinzugegebenen Oxonium-Ionen auf.
- Setze den pH-Wert in die Henderson-Hasselbalch-Gleichung ein und löse zum Quotient der Stoffmengen der Pufferkomponenten auf.
- Rechne das Ergebnis in Prozent um.
- Es handelt sich hierbei um eine Dihydrogenphosphat-Hydrogenphosphat-Pufferlösung, zu der formal Salzsäure gegeben wird.
- Berechne zunächst die Stoffmengen der Pufferkomponenten und der mit der Salzsäure hinzugegebenen Oxonium-Ionen aus und verfahre dann wie in A10.
- Setze den gegebenen pH-Wert in die Henderson-Hasselbalch-Gleichung ein und notiere sinnvoll im Quotienten die Stoffmenge an Oxonium-Ionen, die zugegeben werden muss, aber noch unbekannt ist, um den gewünschten pH-Wert zu erreichen.
- Löse die Gleichung zur Oxonium-Ionen-Stoffmenge auf und berechne zum Schluss, wie viel Salzsäure in mL der angegebenen Salzsäure notwendig wäre, um diese Stoffmenge zu erreichen.
- Überlege noch einmal: Wann puffert ein Puffersystem optimal?
- Welches Puffersystem sollte gewählt werden, damit dieses optimal oder „nahe dran“ bei pH = 6 puffern kann?
- Ein Blick in die pKS-Wertetabelle hilft!
- Überprüfe einmal die pK-Werte des vorgeschlagenen Puffersystems und überlege, ob dieses…
- … eine gute Wahl ist zum Puffern bei einem pH-Wert um 12.
- … die Kriterien eines Puffersystems erfüllt.
