Ein Blick in die Hülle des Atoms
Von der Wolke zur Ordnung – Niels Bohrs Schalenmodell
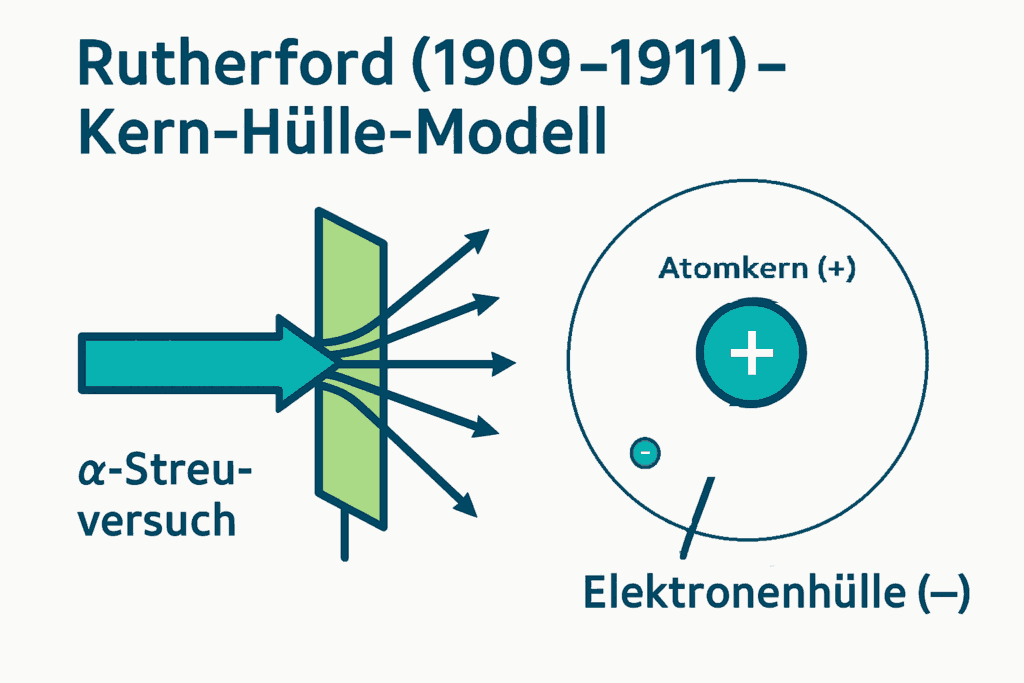
Rutherfords Atommodell hatte eine wichtige Erkenntnis gebracht: Im Zentrum des Atoms sitzt ein winziger, positiv geladener Kern, während die Elektronen sich irgendwo in der Hülle aufhalten. Doch eine entscheidende Frage blieb offen: Wie genau bewegen sich diese Elektronen? Kreisen sie wild durcheinander wie Mücken an einem Sommerabend, oder gibt es eine verborgene Ordnung in ihrem Tanz?
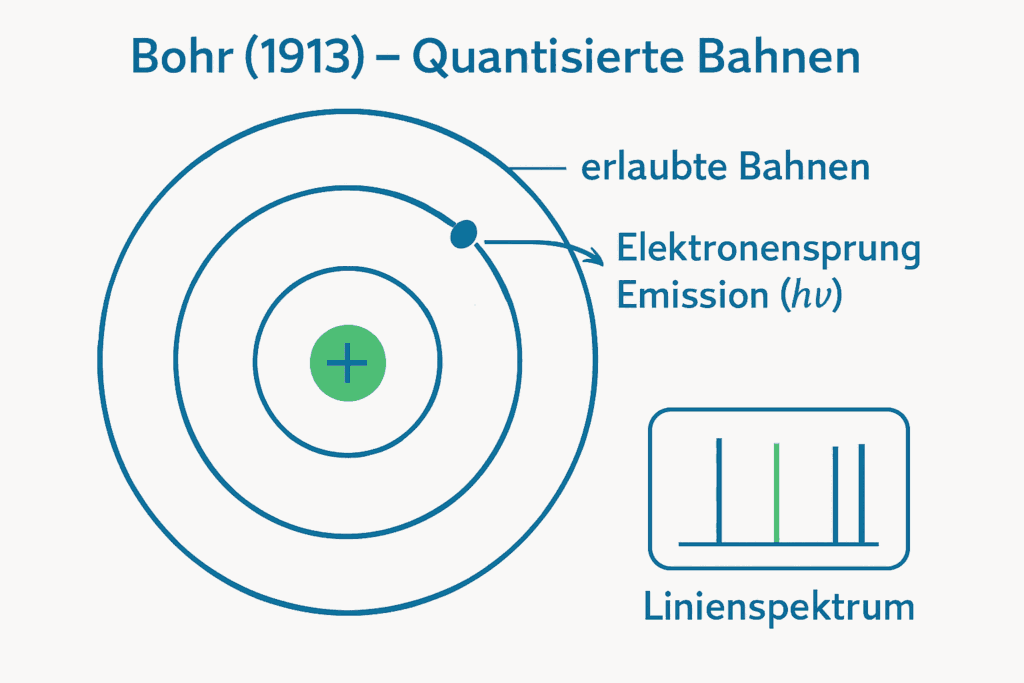
Der dänische Physiker Niels Bohr wagte 1913 einen kühnen Gedanken: Was wäre, wenn die Elektronen nicht beliebig um den Kern kreisen könnten, sondern nur auf ganz bestimmten Bahnen? Ein Elektron könnte nur dann von einer „Schale“ zur nächsten springen, wenn es genau die richtige Menge an Energie aufnimmt oder abgibt.
Der Franck-Hertz Versuch
Nur ein Jahr später, 1914, führten James Franck und Gustav Hertz ein berühmtes Experiment durch, das Bohrs Vorstellung auf verblüffende Weise bestätigte. Ihr Versuch zeigte, dass Atome tatsächlich nur ganz bestimmte Energiemengen aufnehmen können – ein eindeutiger Beweis dafür, dass Elektronen in bestimmten Schalen organisiert sein müssen.
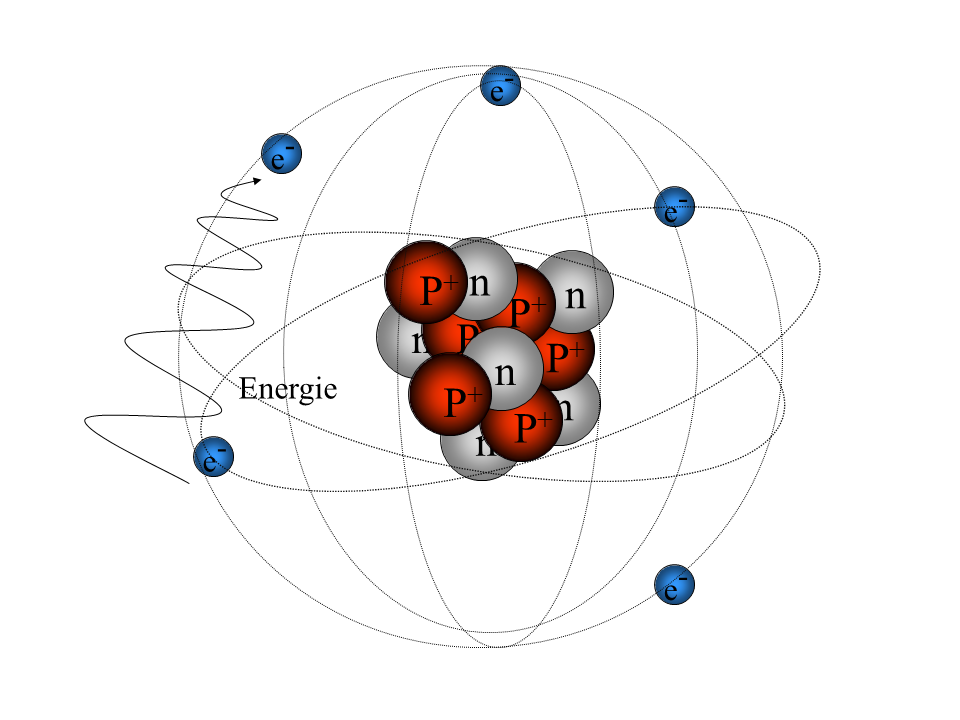
Heute wollen wir diesem Schalenmodell auf die Spur kommen. Dazu werden wir uns theoretisch ansehen, was passiert, wenn man einem Atom seine Elektronen Stück für Stück entreißt – eine Technik, die Ionisierung genannt wird.
Ionisierungsenergien
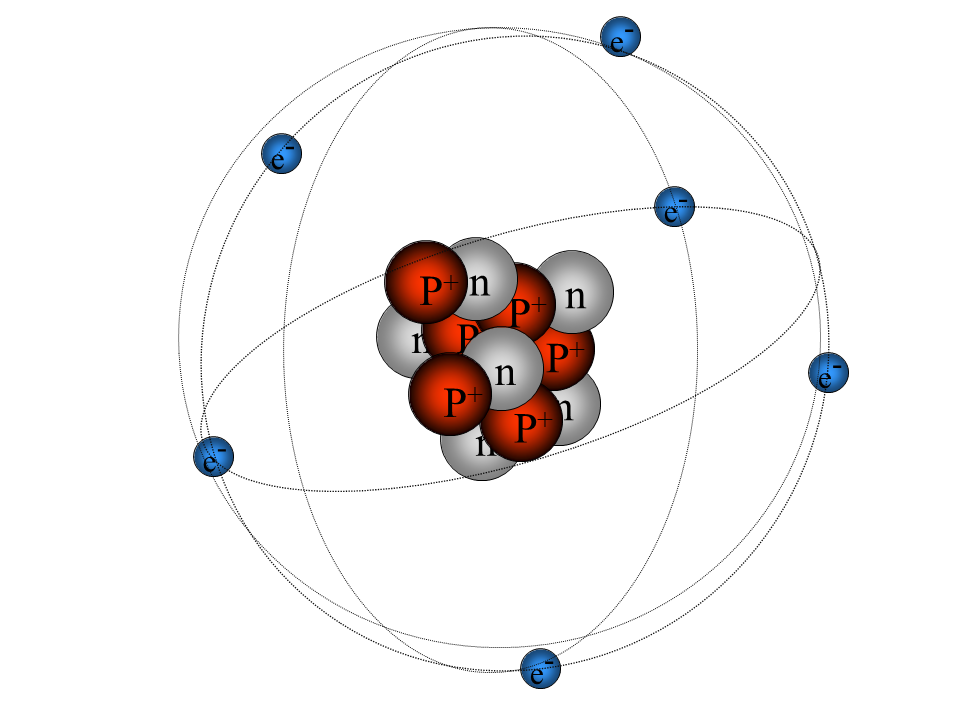
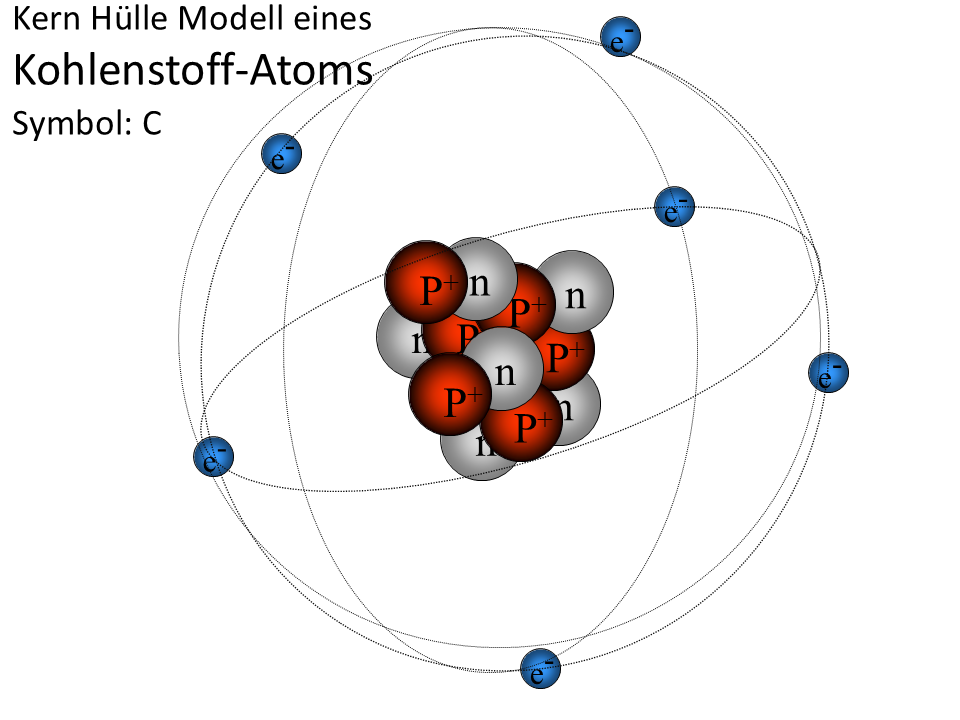
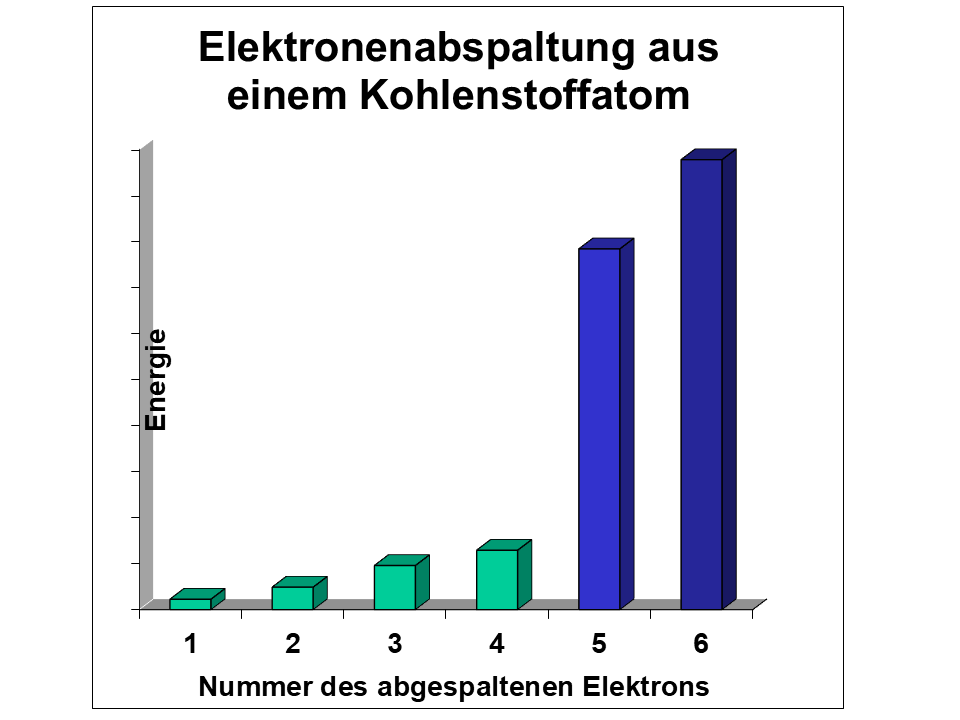
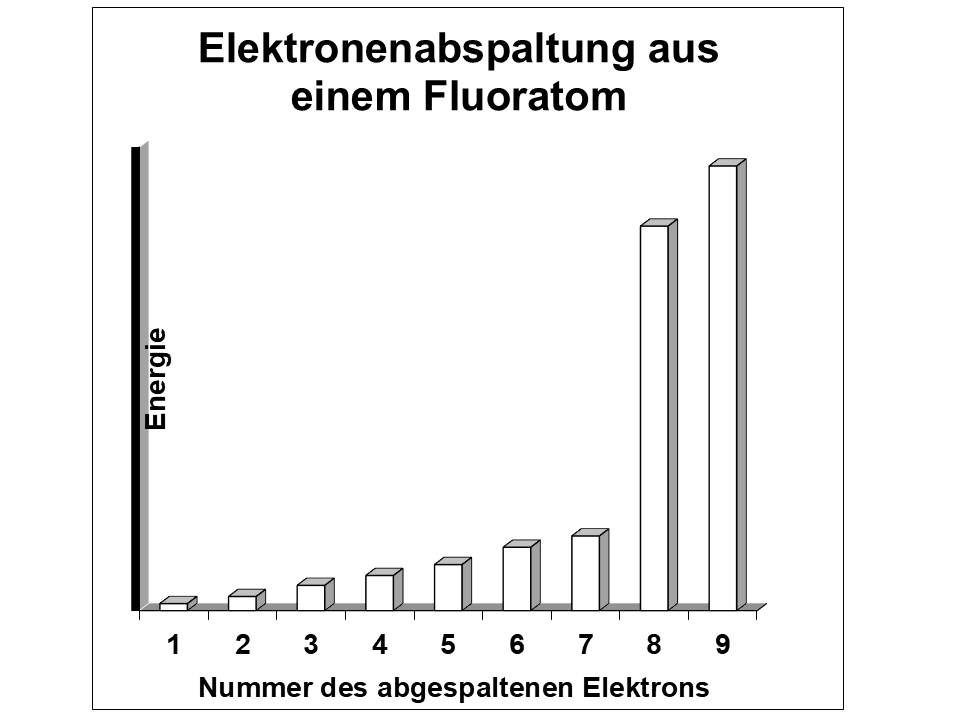
Lass uns das einmal gemeinsam durchgehen. Was könnte auf dem ersten Bild der Galerie 1 modellhaft abgebildet sein?
Ionisierungsenergien und das Schalenmodell.1
Aufgaben
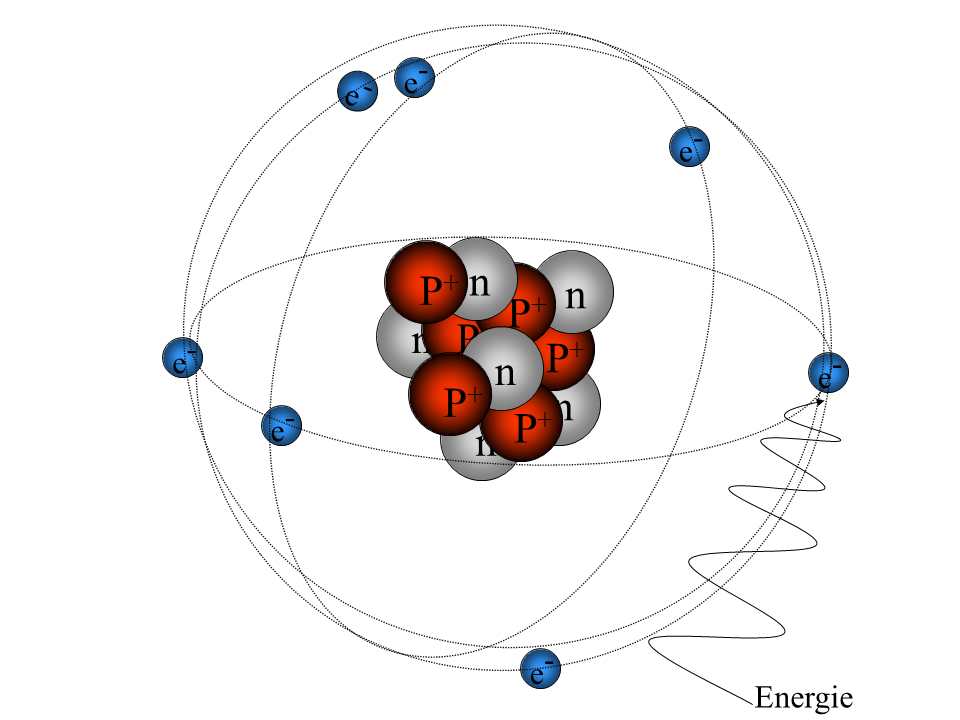
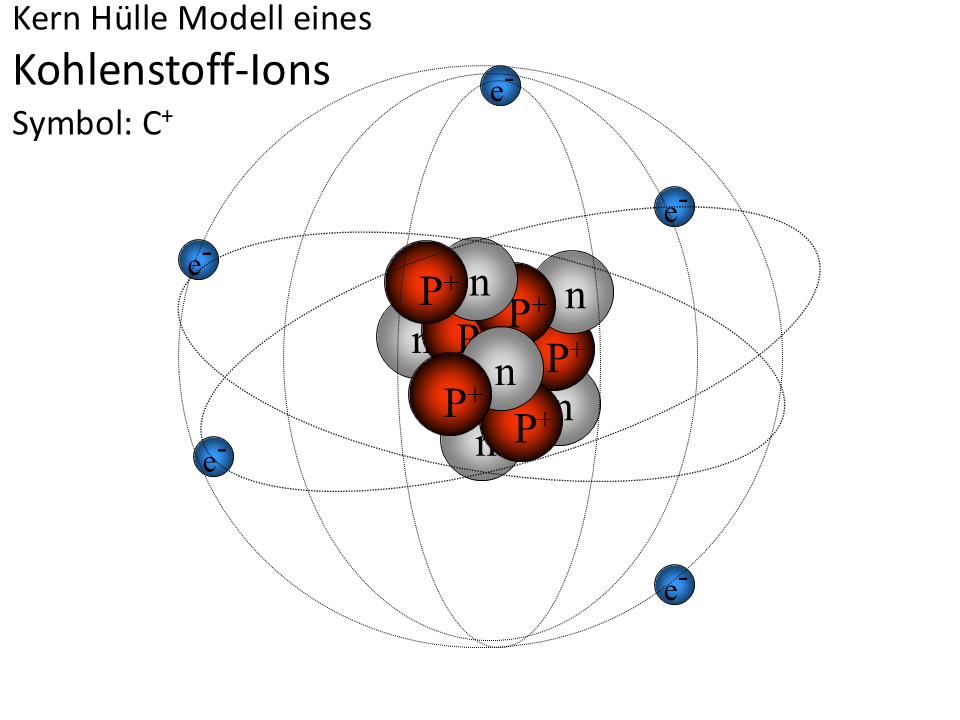
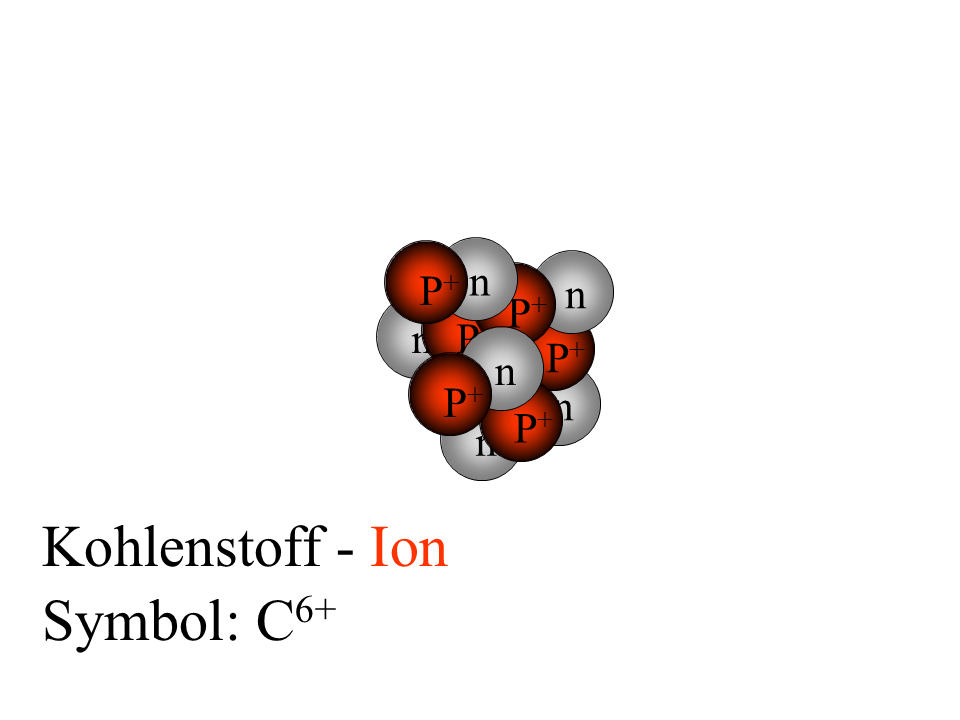
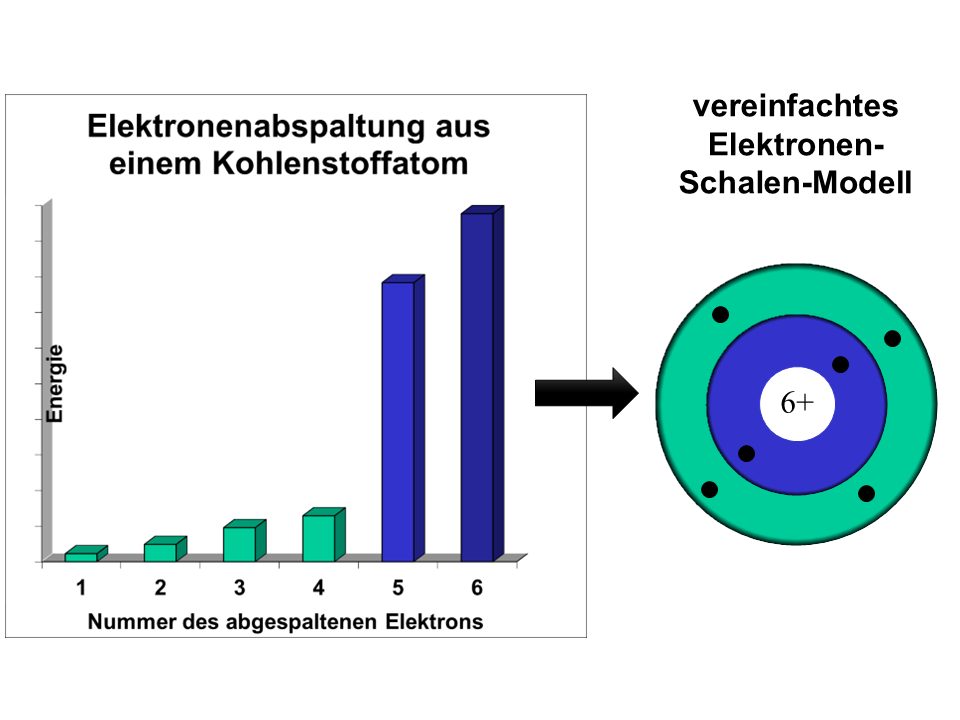
- Wir erfassen gemeinsam die Gedanken M1. Formuliere, was genau auf der letzten Abbildung der Galerie 1 dargestellt ist.
- Kopiere dir die Diagramme aus M2, damit du sie bearbeiten kannst.
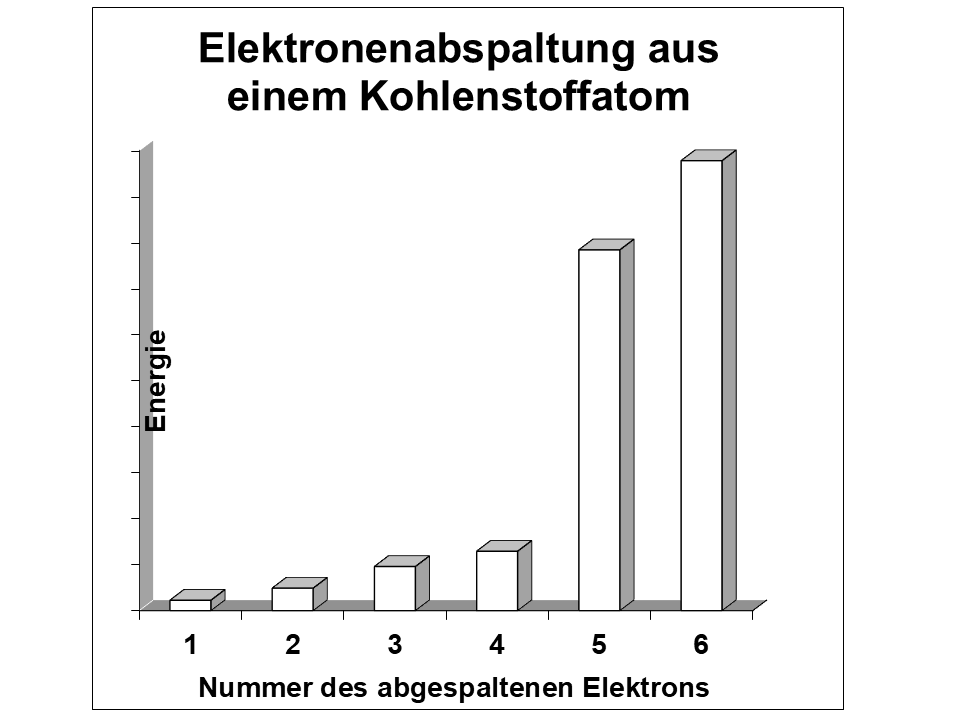
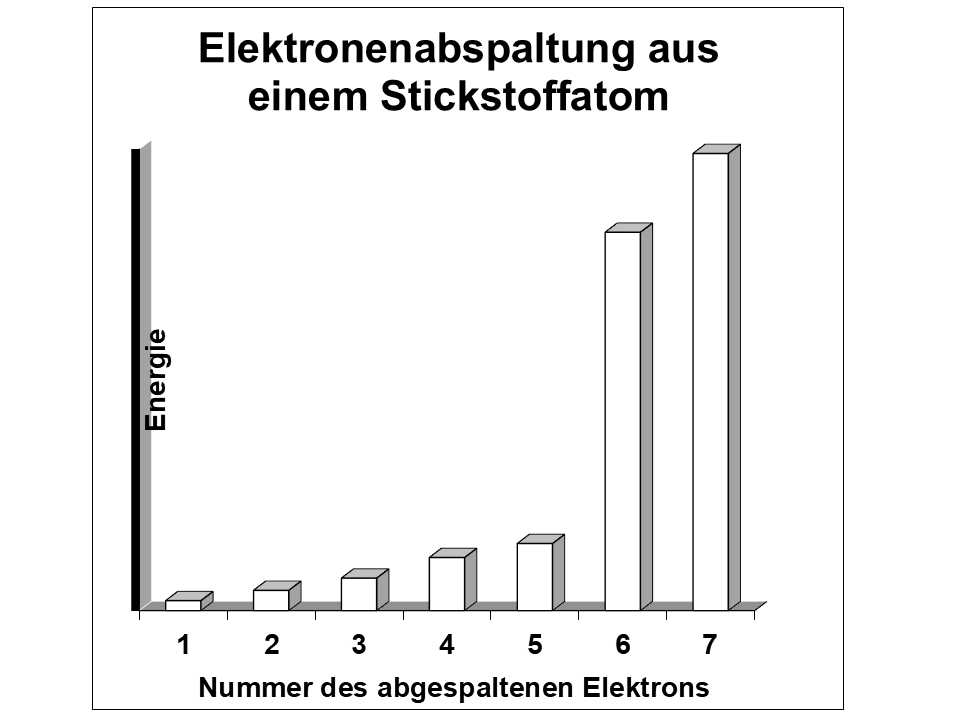
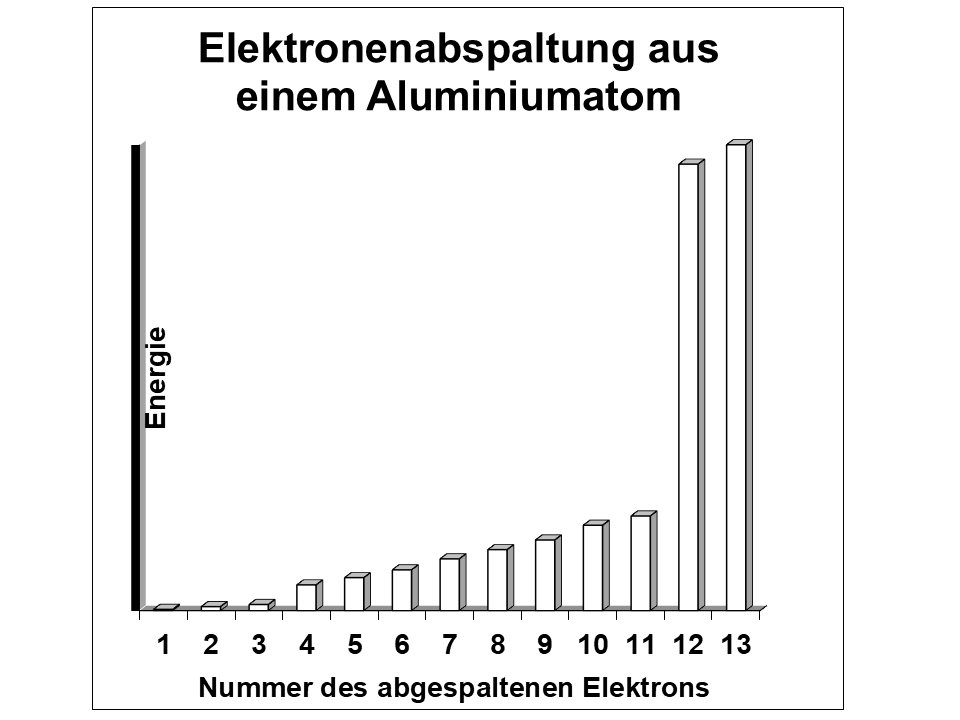
- Vervollständige zuerst die Diagramme der drei Messergebnisse, indem du ähnlich hohe Energien jeweils farbig kennzeichnest! „Energiesprünge“ erkennst du gut, wenn du über die Balkenenden ein Lineal legst.
- Vergleiche deine vervollständigten Diagramme mit denen deines Nachbarn.
- Zeichnet zusammen für alle drei Atome ein Atommodell. Ihr könnt die Vorlagen nutzen, in denen der Kern bereits vereinfacht eingezeichnet wurde. Das Modell muss die Energiesprünge durch unterschiedlich weit vom Kern entfernte Elektronen erklären.
Finden wir Regelmäßigkeiten in der Elektronenhülle?
Weiteres
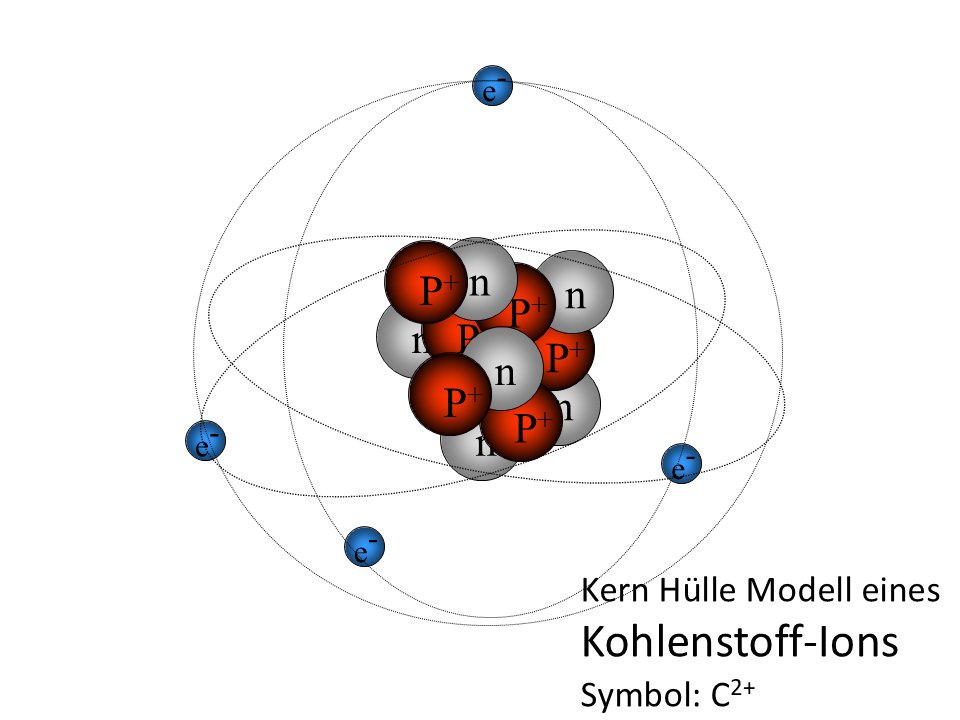
Als Ion bezeichnet man Atome, aus denen Elektronen entfernt wurden. Die Ionisierungsenergie ist also die Energie, die man braucht, um ein Elektron aus der Atomhülle zu entfernen. Hier Daten aller Ionisierungsenergien von drei Atomsorten:
Aufgaben
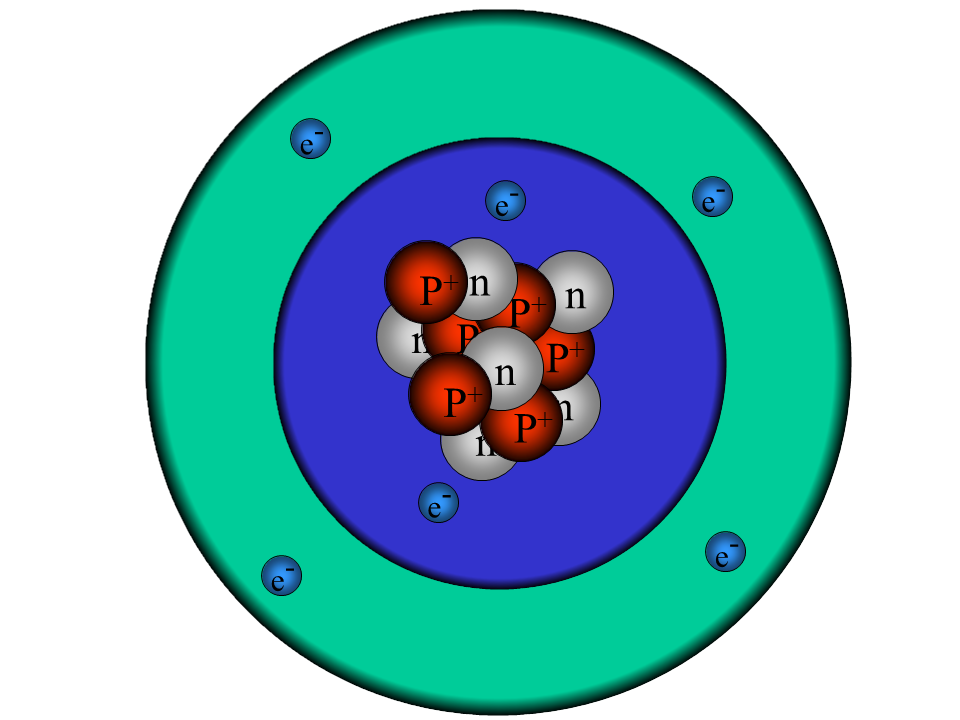
- Lies M3, lade dir die Abb. 2 herunter und ergänze diese mit den fehlenden Kernladungen (innerster Kreis) sowie allen Elektronen (als Punkte zeichnen).
- Wir wissen: Elemente in einer Gruppe reagieren im selben Atomzahlverhältnis mit anderen Elementen. Benenne das Einzige, was Elemente einer Gruppe gemeinsam haben.
Das Schalenmodell und das Periodensystem
Das Schalenmodell nach Bohr
Im Schalenmodell bewegen sich die Elektronen nicht wahllos um den Kern, sondern sie halten sich in bestimmten „Bahnen“ oder Schalen auf. Diese Schalen sind um den Kern angeordnet.
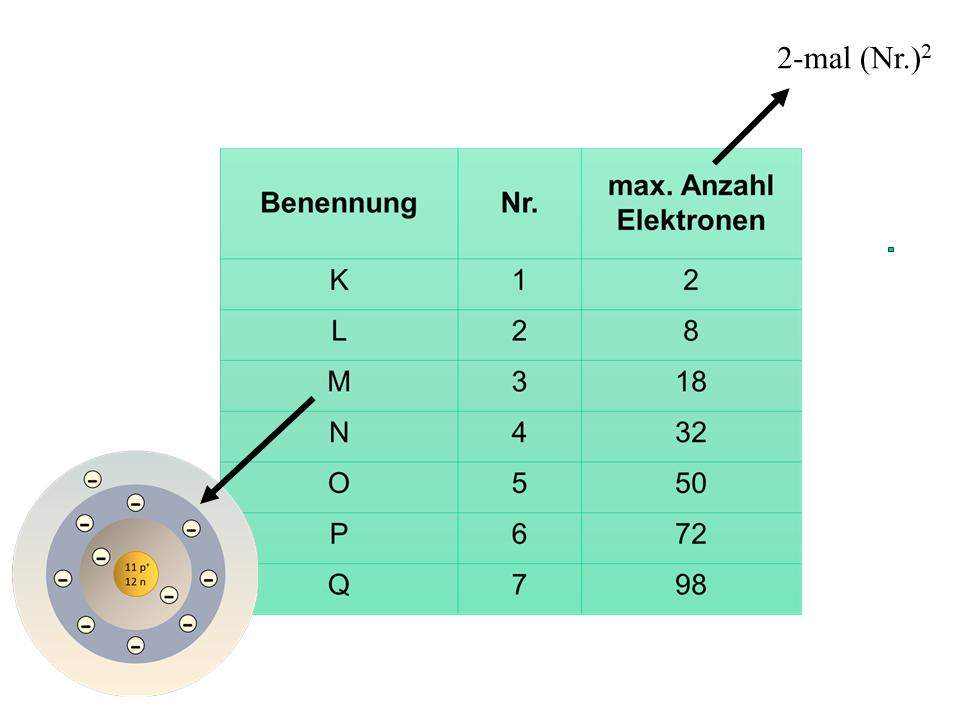
Für uns weniger wichtig ist, dass die innerste, erste Schale mit „K-Schale“, die zweite mit „L-Schale“, die dritte mit „M-Schale“ und so weiter alphabetisch benannt werden.
Wichtig hingegen ist, dass jede Schale nur eine begrenzte Anzahl von Elektronen aufnehmen kann. Die maximale Anzahl an Elektronen pro Schale kann gemäß folgender Formel berechnet werden: Anzahl = 2·n² (mit n = Nummer der Schale).
Schalen und max. Elektronenanzahl.3
Wichtige Grundsätze zur Elektronenverteilung
Die Schalen werden von innen nach außen besetzt.
Für die ersten 18 Elemente gilt: in der äußersten Schale sind nie mehr als 8 Elektronen – auch wenn rechnerisch mehr hineinpassen würden.
Beispiel Natrium: Natrium hat 11 Elektronen. Die Besetzung der Schalen sieht so aus:
K-Schale: 2 Elektronen
L-Schale: 8 Elektronen
M-Schale: 1 Elektron
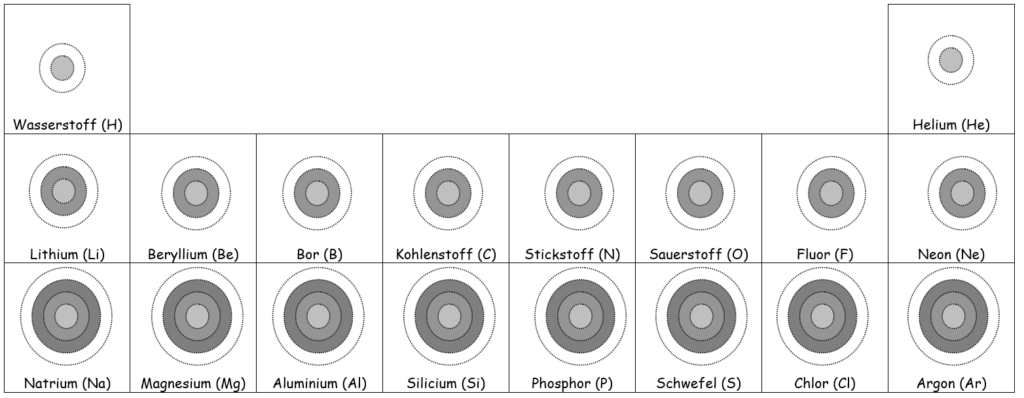
Schalenmodelle der Atome der ersten 18 Elemente
Ergänze die fehlenden Elektronen.4
Was für uns noch wichtig ist
Die Verteilung der Elektronen eines Atoms auf die Schalen nennt man Elektronenkonfiguration.
Im Periodensystem endet eine Periode immer mit einem Edelgas. Bei den Atomen der Edelgase ist immer die äußerste Schale mit Elektronen gefüllt.
Dann entspricht ja logischerweise die Nummer der Periode, in der ein Element steht, der Anzahl der Schalen seiner Atome, oder?
Ja, und was vielleicht noch wichtiger ist, ist die Tatsache, dass die Atome der Elemente in einer Gruppe immer dieselbe Anzahl an Elektronen in der äußersten Schale (Valenzelektronen) haben!
Die Elektronenkonfiguration erklärt die Stellung der Elemente im Periodensystem. Mit der Kenntnis der Anzahl der Valenzelektronen kann man vorhersagen, wie Atome miteinander reagieren.
Weitergedacht
- Verschaffe dir einen Überblick und entnimm M4 die wichtigsten Informationen. Stelle stichwortartig zusammen, was die jeweiligen Atommodell an neuen Aussagen mach(t)en und wofür wir sie nutzen können.
- Schreibe drei „Take home messages“ zum Schalenmodell auf.
- Willst du es nochmal anders erklärt bekommen? Dann schau dir M5 an.
- M6 ist für alle, die es genau wissen wollen.
Überblick - Ausblick
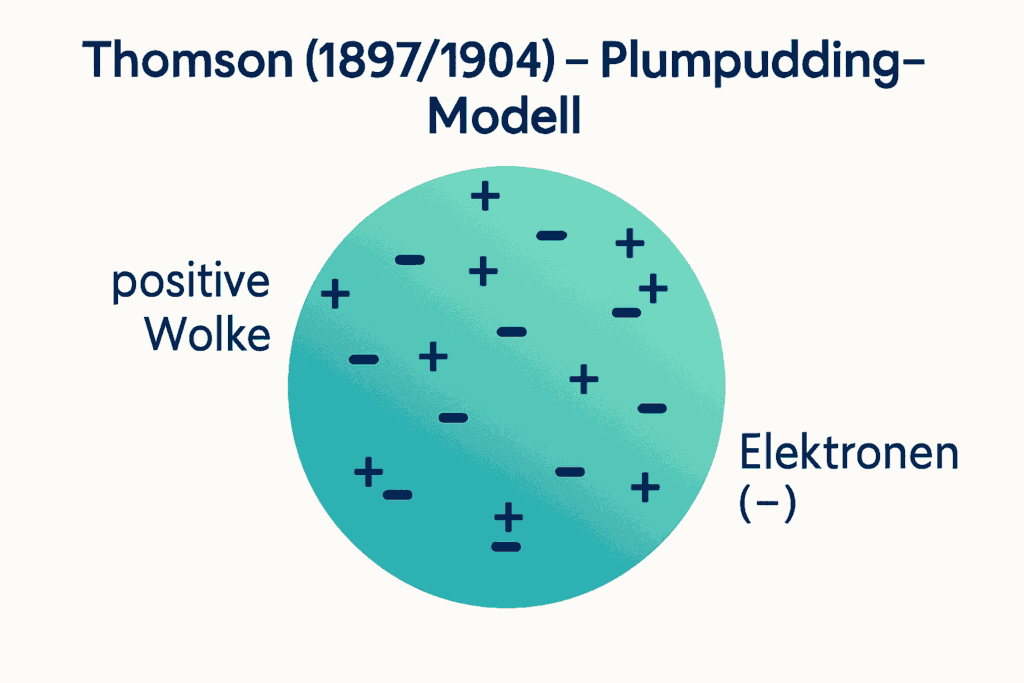
Unsere bisherigen Modelle im Überblick
Diverse Atommodelle5
Warum uns die äußerste Schale am meisten interessiert
Nun müssen wir ehrlich sein: Das Schalenmodell nach Bohr ist nicht das Ende der Geschichte. Die Wissenschaft hat inzwischen weiterentwickelte und noch genauere Atommodelle hervorgebracht. Doch für uns als Chemikerinnen und Chemiker ist vor allem eines entscheidend: die äußerste Elektronenschale eines Atoms.
Warum gerade diese? Die Antwort ist einfach: Chemie ist die Wissenschaft der Begegnungen. Wenn Atome aufeinandertreffen und miteinander reagieren, dann geschieht diese Wechselwirkung fast ausschließlich über ihre äußerste Schale – dort, wo sie sich sozusagen „berühren“ können. Die inneren Schalen bleiben bei chemischen Reaktionen in der Regel unangetastet.
Deshalb hat diese besondere Schale auch einen eigenen Namen erhalten: die Valenzschale. Der Begriff stammt vom lateinischen Wort valere, was „gelten“ oder „von Bedeutung sein“ bedeutet – und genau das ist sie: die Schale, die wirklich zählt, wenn es um chemische Bindungen und Reaktionen geht.
Wo geht es hin?
Wir werden noch einen Schritt weiter gehen, da uns die Valenzschale besonders interessiert. In dieser Schale können wir uns kleine Räume für jeweils immer zwei Elektronen vorstellen.
Dies zeigt das Kugelwolkenmodell auf Schulniveau sehr gut. Dieses Modell werden wir bald verwenden.
Wer viel weiter gehen will, kann sich eigenständig über das Orbitalmodell informieren.
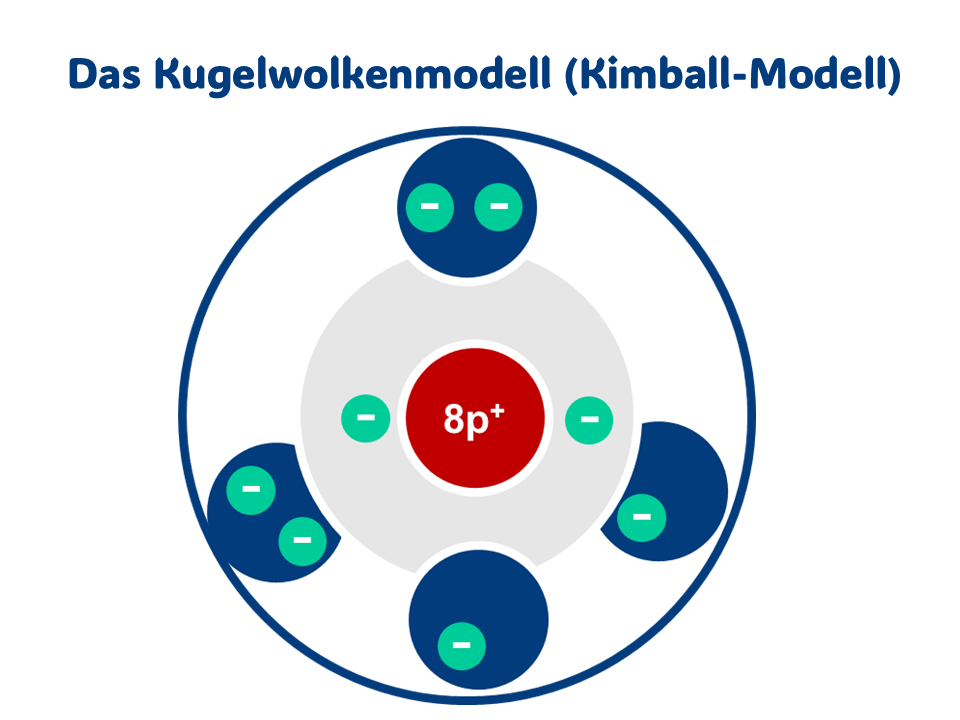
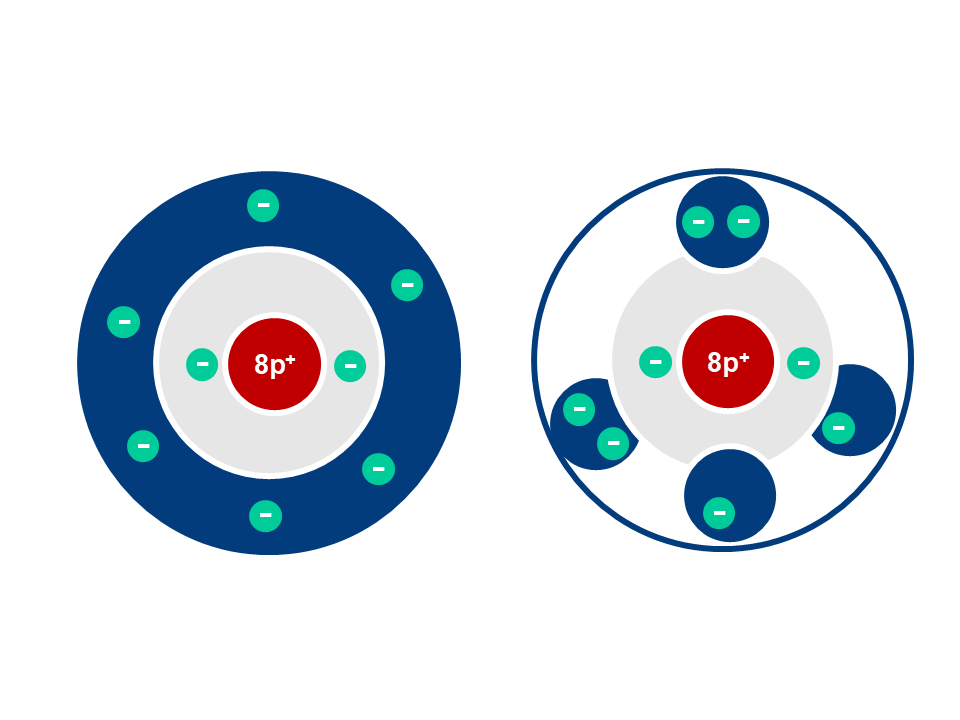
Hin zum Kugelwolkenmodell.5
Weiteres
Wir werden mit diesem Modell sehr gut verstehen können, wie Atome sich zu Molekülen verbinden.
Das Schalenmodell von einer Wissenschaftlerin für Lernende erklärt
Weiteres
Mai Thi Nguyen-Kim erklärt es für uns
Hinweise zum Video
Bis 02:27 zeigt das Video eine Wiederholung des Kern-Hülle-Modells.
Bei 05:10 wird gesagt, dass die Schalen immer von innen nach außen gefüllt sind. Dies gilt nur für die Elemente mit der Protonenanzahl 1-18. Danach gibt es eine Sonderregel in Bezug auf die Elektronenverteilung (siehe M6).
Elektronenkonfiguration für Fortgeschrittene
Die "Nebengruppen" im Blick
Bei Elementen mit der Protonenanzahl größer als 18 können andere Regeln in Bezug auf die Verteilung der Elektronen und Anzahl der Außenelektronen gelten
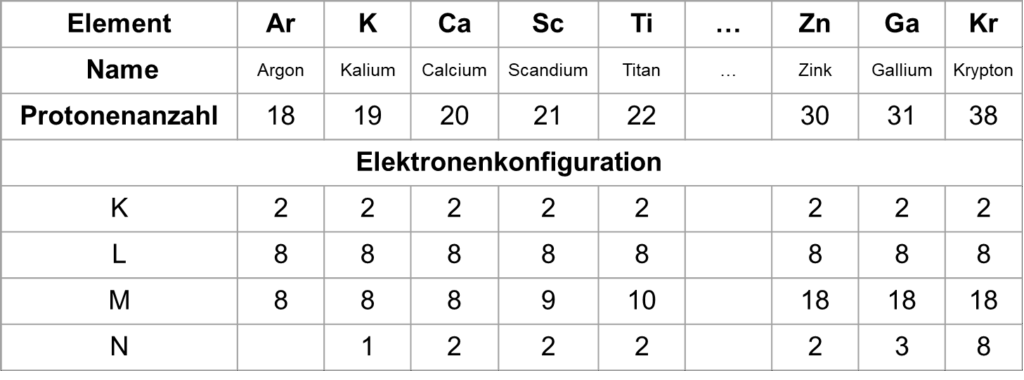
Die folgende Tabelle zeigt einen Auszug der Elektronenkonfiguration der Elemente mit der Protonenanzahl 18 bis 38
Verteilung der Elektronen.6
Bei den Nebengruppenelementen kommen Element für Element immer mehr Elektronen in einem Bereich einer inneren Schale hinzu. Bei den Elementen mit der Protonenzahl 19-38 gilt die N-Schale als Außenschale.
Wir merken uns
Im deutschen Sprachraum unterteilt man das Periodensystem häufig in Hauptgruppen und in Nebengruppen.
Bei den Atomen aller Elemente der Hauptgruppen stimmt die Anzahl der Valenzelektronen mit der Nummer der Hauptgruppe überein.
In Atomen der Elemente der Nebengruppen kommen Element für Element weiter innen Elektronen hinzu und füllen hier Räume auf. Daher haben diese Atome allesamt nur wenige Außenelektronen. Die zugehörigen Stoffe sind übrigens allesamt Metalle. Warum, werden wir noch sehen.