Aufgaben
- Beobachten Sie den Lehrerversuch V1 genau und vollziehen Sie im Anschluss seine Hintergründe in M1 nach.
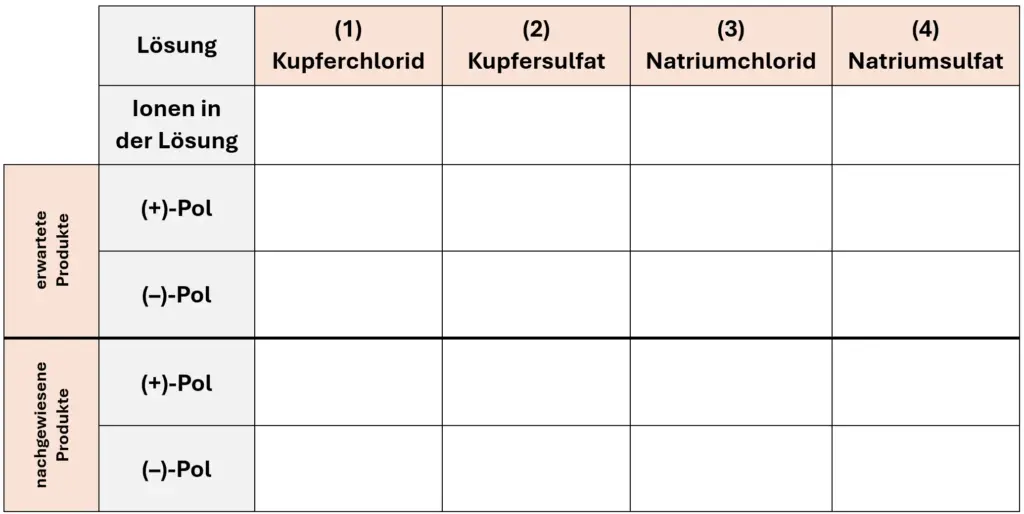
- Stellen Sie in M2 Vermutungen auf, welche Produkte entstehen, wenn man jeweils eine wässrige Lösung aus Kupferchlorid, Kupfersulfat, Natriumchlorid und Natriumsulfat elektrolysiert und geben Sie mögliche Nachweisversuche an.
- Beobachten Sie den Lehrerversuch V2 genau und notieren Sie ihre Beobachtungen in M2.
- Notieren Sie basierend auf ihren Beobachtungen und hiervon abweichender Vermutungen für die Elektrolyse der verschiedenen Salzlösungen jeweils ein eigenes Redoxschema.
- Notieren Sie zu allen Teilgleichungen ihrer Redoxschemata das jeweilige Standardelektrodenpotential. Vergleichen Sie für jede Elektrolysezelle die Standardelektrodenpotentiale mit ihren Vermutungen, die nicht stattgefunden haben und formulieren Sie eine Schlussfolgerung.
Eine Zink-Iodid-Lösung elektrolysieren
Materialien
- Schutzbrille
-
Becherglas
- falls die Zinkiodid-Lösung angesetzt werden muss
-
U-Rohr
- ggf. mit Fritte
-
Stativmaterial
- mit Stativklemme und -muffe
- 2 Graphitelektroden
- Elektrischer Motor
- Anlaufspannung 2 mA
- 2 Kabel
- 2 Krokodilklemmen
- Spannungsmessgerät
- Mutimeter
- Gleichspannungsquelle
Chemikalien
-
Zinkiodid
- oder fertige Zinkiodid-Lösung
- 2 Graphit-Elektroden
-
Natriumthiosulfat-Lösung
- Zur Reduktion überschüssigen Iods
Durchführung
- Falls keine fertige Zinkiodid-Lösung aus einem Vorratsgefäß vorliegt: 1,5 g Zinkiodid in 50 mL dest. Wasser geben. Ein eventuell entstehender weißer Niederschlag durch Zugabe von ein paar Tropfen Salzsäure wieder auflösen.
- Die Lösung in ein U-Rohr (mit Fritte) füllen und dieses an einem Stativ befestigen.
- Den Akkumulator aufladen: Die Elektroden mit einer Gleichspannungsstromquelle verbinden. An der Spannungsquelle ein Spannungsmessgerät parallel schalten. Bei 3 V so lange elektrolysieren, bis deutlich zu erkennen ist, dass sich Iod an der Anode und elementares Zink an der Kathode abscheidet.
- Mit Hilfe des Spannungsmessgeräts die Spannung und die Stromstärke messen.
- Mit Hilfe dieser Zelle einen elektrischen Motor in Betrieb nehmen.


Vorher und Nachher beim Aufladen des Zink-Iod-Akkumulators.
Entsorgen und Aufräumen
-
Die Lösung in eine Vorratsflasche, in der sich etwas Zink im Überschuss befindet, aufbewahren. Das restliche Iod reagiert dann zu Iodid. Die Lösung kann dann für die nächste Durchführung aufbewahrt werden oder über dem Sammelbehälter für Schwermetallsalze entsorgt werden.
-
Das U-Rohr mit Natriumthiosulfat-Lösung spülen und so überschüssiges Iod zu Iodid reduzieren. Dann über dem Ausguss entsorgen. Alle verunreinigte Labormaterialien spülen.
-
Alle Materialien an ihren Ursprungsort zurückstellen.
Hintergründe zu V1
Bei der Elektrolyse wird elektrische Energie genutzt, um eine unfreiwillige Redoxreaktion zu erzwingen. Dabei wird elektrische Energie in chemische Energie umgewandelt. Dies nutzt man bei Akkumulatoren aus.
Akkumulatoren sind wiederaufladbare Batterien, auch Sekundärbatterien genannt. In Abgrenzung dazu existieren Primärbatterien. Das sind nicht wiederaufladbare Batterien.
Als Elektrolysezelle
Zu Beginn haben wir eine Gleichspannungsquelle genutzt, um eine Zink-Iodid-Lösung zu elektrolysieren. Dabei finden folgende Prozesse statt:
Elementares Iod wird in Form von braunen Schlieren an der Anode (hier der Plus-Pol) sichtbar. An der Kathode (hier der Minus-Pol) scheidet sich elementares Zink ab. Das Zelldiagramm dieser Elektrolysezelle sieht wie folgt aus:
Als galvanische Zelle
Nach der Elektrolyse wurden die Elektroden des Aufbaus mit einem Verbraucher verbunden. Dabei finden folgende Prozesse statt:
Elementares Zink wird an der Anode (hier der Minus-Pol) oxidiert und elementares Iod wird an der Kathode (hier der Plus-Pol) zu Iodid reduziert. Das Zelldiagramm dieser galvanischen Zelle sieht wie folgt aus:
Elektrolyse verschiedener Salzlösungen
Wir haben soeben gesehen, dass sich Zinkiodid-Lösung elektrolysieren lässt. Dabei entstehen an den Elektroden elementares Zink und Iod. Überlege Dir, welche Stoffe an den Elektroden bei einer Elektrolyse der folgenden Salzlösungen entstehen könnten.
Elektrolyse verschiedener Salzlösungen
Materialien
- Schutzbrille
- Abzug
-
Stativmaterial
- mit Stativklemme und -muffe
-
U-Rohr mit seitlichem Ansatz
- Fritte optional
- 2 Graphitelektroden
- 2 Kabel
- 2 Krokodilklemmen
- Spannungsmessgerät
- Mutimeter
- Gleichspannungsquelle
Chemikalien
- Kupferchlorid 0,1 mol/L
- Kupfersulfat 0,1 mol/L
- Natriumchlorid 0,1 mol/L
- Natriumsulfat 0,1 mol/L
Sicherheitshinweis
Bei der Elektrolyse entstehen u.a. giftige Gase, weshalb der Versuch unter dem Abzug durchgeführt wird.
Durchführung
- Das U-Rohr an ein Stativ befestigen und unter dem Abzug stellen.
- Das U-Rohr nacheinander mit 50 mL der Salzlösungen befüllen. Zwischen den Befüllvorgängen das U-Rohr spülen.
- Analog zur Elektrolyse von Zinkiodid eine Gleichspannungsquelle über Graphitelektroden anschließen und die Lösung elektrolysieren.
- Entstandene Produkte mithilfe bekannter Nachweisverfahren prüfen.
Entsorgen und Aufräumen
-
Entstandenes gelöstes Chlorgas durch die Zugabe überschüssiger Mengen Natriumthiosulfats reduzieren. Kaliumiodid-Stärkepapier nutzen, um auf Chlorgasrückstände zu testen (positiv: blau/violett-Färbung). Dann alle Lösungen in den Entsorgungsbehälter für Schwermetallsalze geben.
-
Alle verunreinigten Labormaterialien spülen.
-
Alle Materialien an ihren Ursprungsort zurückstellen.
Weitergedacht
- Erklären Sie den Sinn und Zweck eines Diaphragmas bei Elektrolysen am Beispiel der Elektrolyse von Zinkiodid.