Willkommen
- Schau dich im Labor M1 von Ernest Ruhterford ein wenig um.
- Mache dich dann zunächst mit der Idee und dem Aufbau des Versuchs vertraut. Wichtig für das Verständnis ist der mögliche Weg der alpha-Teilchen: Radium -> Goldfolie -> Aufprall auf einem Detektor
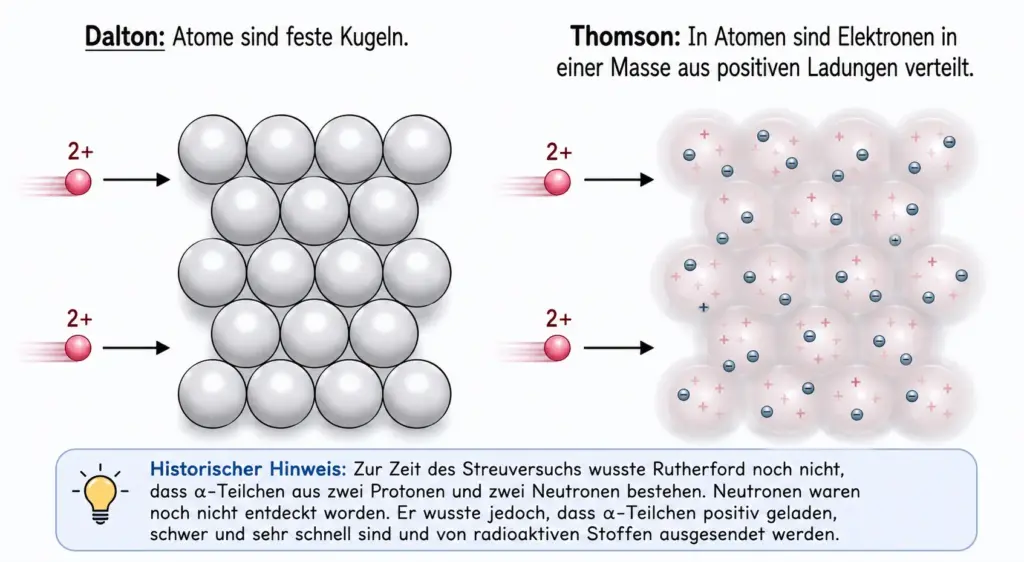
- Stell dir vor, du bist Forscherin oder Forscher im Jahr 1909 – und weißt noch nicht, was der Versuch zeigen wird. Die alpha-Teilchen treffen in der Goldfolie auf sehr viele Goldatome. Was würde mit ihnen passieren? Schau dir Abb. 2 an und formuliere für jedes Modell deine Erwartung in einem Satz:
- „Nach dem Dalton-Modell erwarte ich, dass die alpha-Teilchen …, weil …“
- „Nach dem Thomson-Modell erwarte ich, dass die alpha-Teilchen …, weil …“
- Vergleiche deine Erwartungen zu dem Versuch mit denen Rutherfords und seiner Mitarbeiter aus M1.
Manchester im Jahr 1909
Zu Besuch bei einem berühmten Forscher
Ernest Rutherfords Labor zu Beginn des 20. Jahrhunderts.1
Im abgedunkelten Labor an der Universität Manchester herrscht konzentrierte Ruhe. Ernest Rutherford lässt seine Mitarbeiter Hans Geiger und Ernest Marsden geduldig winzige Lichtblitze zählen. Die drei wollten herausfinden, was passiert, wenn sogenannte alpha-Teilchen auf eine sehr dünne Schicht Atome trifft.
Die handelnden Personen
Der aus Neuseeland stammende Physiker Ernest Rutherford gehört zu den bedeutendsten Forschern der Atomphysik. Zunächst untersuchte er radioaktive Strahlung und erkannte, dass es verschiedene Arten von Strahlung gibt, darunter die Alpha-Strahlung. Aus den für ihn überraschenden Ergebnissen des hier vorgestellten Versuchs entwickelte er 1911 das Kern-Hülle-Modell des Atoms.
Für seine Forschungen zur Radioaktivität erhielt er bereits 1908 den Nobelpreis für Chemie.
Rutherford scherzte später selbst darüber, dass er als Physiker den Nobelpreis für Chemie erhalten hatte. Sinngemäß sagte er, er sei plötzlich „in einen Chemiker verwandelt worden“.2
Hans Geiger arbeitete in Manchester eng mit Ernest Rutherford zusammen. Er entwickelte sehr genaue Methoden, um Alpha-Teilchen nachzuweisen und ihre Ablenkung zu messen. Gemeinsam mit Ernest Marsden führte er die berühmten Streuversuche an dünnen Metallfolien durch.
Im Ersten Weltkrieg diente Geiger übrigens danach als Artillerieoffizier auf deutscher Seite. Er überlebte den Krieg und setzte seine Forschung zur Radioaktivität fort . Später entwickelte er noch gemeinsam mit Walther Müller das berühmte Geiger-Müller-Zählrohr. Mit diesem Gerät kann radioaktive Strahlung nachgewiesen werden.
Ernest Marsden war zur Zeit des Streuversuchs noch ein sehr junger Physikstudent. Zusammen mit Hans Geiger untersuchte er, wie Alpha-Teilchen durch Goldfolie abgelenkt werden.
Im Ersten Weltkrieg diente Marsden später auf britischer Seite in einer technischen Einheit zur Ortung feindlicher Geschütze.
Man sieht: Forschung ist international – aber dies bewahrt Menschen nicht immer davor, auf unterschiedlichen Seiten in einem Krieg eingesetzt zu werden.
Was würdest du erwarten, wenn ...?
Zwei denkbare Modelle: Alphastrahlen treffen auf Atome – was wird passieren?3
mehr zur alpha-Strahlung
Ernest Rutherford nutzte die Alpha-Teilchen, um Atome „abzutasten“. Er und sein Team wussten, dass Alpha-Teilchen positiv geladen, viel schwerer als Elektronen und sehr schnell sind. Deshalb eigneten sie sich gut, um den Aufbau von Atomen zu untersuchen.
Was er nicht wusste, wir heute ab genauer wissen:
Alpha-Teilchen bestehen aus 2 Protonen und 2 Neutronen. Sie entsprechen damit dem Kern eines Heliumatoms. Da zwei positiv geladene Protonen enthalten sind, sind Alpha-Teilchen insgesamt zweifach positiv geladen. Die Neutronen wurden erst 1932 von James Chadwick entdeckt.
Die Geschichte der Alpha-Strahlung ist eng mit der Entdeckung der Radioaktivität verbunden.
Den ersten Schritt machte 1896 der französische Physiker Henri Becquerel. Er entdeckte zufällig, dass Uran von selbst eine unsichtbare Strahlung aussendet, die eine „Fotoplatte“ schwärzt.
Marie Curie und Pierre Curie untersuchten diese Strahlung genauer. Sie prägten den Begriff „Radioaktivität“ und entdeckten sogar weitere stark strahlende Stoffe wie Polonium und Radium.
Erst Ernest Rutherford erkannte dann, dass radioaktive Strahlung nicht einheitlich ist. Um 1899 stellte er fest, dass es verschiedene Arten von Strahlung gibt. Er unterschied zunächst:
- Alpha-Strahlung
- Beta-Strahlung
Später kam noch die Gamma-Strahlung hinzu.
Eine umfassende Würdigung von Marie Curie würde Bücher füllen. In Kürze soll hier hervorgehoben werden, wie ihre Forschung die Experimente von Ernest Rutherford zur Alpha‑Strahlung vorbereitete.
- Marie Curie entwickelte präzise Messverfahren und machte radiumhaltige Präparate verfügbar, die als starke, verlässliche Quellen für Alpha‑Teilchen dienten. Genau solche Quellen nutzten Rutherford und seine Mitarbeiter, um Atome zu „sondieren“.
- Sie zeigte, dass Radioaktivität eine Eigenschaft der Atome selbst ist – nicht eine Wirkung äußerer Einflüsse. Radium sendet „von alleine“ besonders intensive Alpha‑Strahlung aus.
Damit legten Curies Arbeiten zwei Grundlagen für Rutherfords Durchbruch: sie gab im verlässliche Alpha‑Quellen an die Hand und das Verständnis, dass Strahlung im Innersten der Atome entsteht und man damit Atome untersuchen konnte.
Was dachte Rutherford vor dem Experiment?
Seine Forscherfrage
Anklicken zum ÖffnenRutherford wollte das damals herrschende Atommodell von J.J. Thomson überprüfen. Thomson nahm an, dass Atome Elektronen enthalten und dass deren negative Ladung durch eine gleich große, irgendwie diffus verteilte positive Ladung ausgeglichen wird. Er stellte sich das Atom folglich als gleichmäßig positiv geladene Kugel vor, in der Elektronen wie Rosinen stecken – das sogenannte „Rosinenkuchenmodell“. In diesem Modell wäre die positive Ladung so weit verteilt, dass sie ein Alpha-Teilchen allenfalls um wenige Grad ablenken könnte. Rutherford wollte diese kleinen Ablenkungen vermessen.
Seine Erwartung
Anklicken zum ÖffnenEr rechnete mit ganz geringen Ablenkungen. Das hatte Thomson rechnerisch vorhergesagt, und Rutherfords eigene erste Versuche schienen das zu bestätigen.
Seine Ahnungen
Anklicken zum ÖffnenGeiger hatte in früheren Messungen jedoch schon etwas mehr Streuung beobachtet als das Modell vorhersagte. Das ließ Rutherford nicht ganz los. Fast beiläufig – als eine Art Übungsaufgabe für den Studenten Marsden – wies er ihn an, auch einmal zu schauen, ob überhaupt irgendein Alpha-Teilchen in großem Winkel zurückgeworfen wird. Er erwartete: nichts.
Das bahnbrechende Experiment
Damit du den Versuch besser nachvollziehen kannst, haben wir in M2 einmal eine Animation dazu erstellt. In Partnerarbeit könntet ihr die folgende Beschreibung und die Animation nebeneinander legen und gleichzeitig zusammen betrachten.
Hans Geiger und Ernest Marsden hatten in dem Labor folgendende Versuchapparatur aufgebaut:
- In einem Bleiblock lag ein Radiumpräparat.
- Durch eine winzige Öffnung kam eine schwache Strahlung aus sogenannten Alpha-Teilchen,
- die auf eine hauchdünne Goldfolie gelenkt wurden.
- Hinter der Goldfolie war noch ein Leuchtschirm mit Zinksulfid (ZnS) als Detektor aufgebaut. Stieß ein Alpha-Teilchen auf den Leuchtschirm, blitzte dieser kurz auf.
- Da Geiger und Marsden die Blitze mit bloßem Auge nicht genau genug sahen, war hinter dem Leuchtschirm ein Mikroskop, das sie bewegen konnten.4
Weiteres
Geiger und Marsden begannen ihre Beobachtungen hinter der Goldfolie.
Dann platzierten sie das Mikroskop in einem anderen Winkel zur Folie – und zählten erneut.
So arbeiteten sie sich stundenlang Winkel für Winkel um die gesamte Folie herum.
Beide notierten wahrscheinlich in einer Skizze auf einem Papier die Treffer pro Position.
Durchführen und beobachten
- Mache dich mit der Handhabung der Animation vertraut und führe damit „fiktive Messungen“ durch. Beginne in der Detektor Standardansicht ZnS Schirm, schalte das Mikroskop dazu und belichte später auch den Fotofilm.
- Halte das Trefferbild (z. B. in Form des entwickelten Fotos) in deinen Unterlagen fest und beschreibe es: Wo gibt es überall Blitze/Punkte und wo häufen sie sich?
- Erstelle vom Versuchsaufbau ein Bildschirmfoto und zeichne in diese Versuchsskizze einige typische Flugbahnen der Alpha-Teilchen, die sich aus dem Trefferbild ableiten lassen.
- Gleiche die Erwartung aus Aufgabe 1 mit den Ergebnissen ab. Lies dazu auch M3. Erkläre, warum der Versuch später „Streuversuch“ genannt wurde.
Animation des berühmten Streuversuch
Weiteres
Der Streuversuch von Rutherford (1909)
Punkteverteilung ähnlich der Messung von Geiger & Marsden (1909)
Animation des Versuchs: links die Strahlen-Quelle (Radium), in der Mitte die Goldfolie, rechts der Leuchtschirm mit dem Mikroskop dahinter5
Handhabung der Animation
Probiere die Animation einfach aus – sie ist selbsterklärend. Verändere die Winkelposition des Mikroskops, schalte zwischen den verschiedenen Ansichten um und schau, was passiert.
Falls du nicht weiterkommst oder bestimmte Funktionen gezielt nutzen möchtest, findest du hier Anleitungen dazu.
Denke an die Aufgabe von Rutherford an Marsden!
Geiger und Marsden saßen im abgedunkelten Labor und zählten winzige Lichtblitze auf einem Leuchtschirm – stundenlang. Um die Blitze besser erkennen und zählen zu können, schauten sie dabei durch ein Mikroskop.
Das kannst du in der Animation nachvollziehen.
- stelle die Radiumquelle → EIN
- der Detektor steht auf ZnS-Schirm (Standardeinstellung)
- nutze die Ansicht → Blick ins Mikroskop einschalten
- Wähle unter „Position Mikroskop“ verschiedene Winkel aus.
Marsden und Geiger haben über einen langen Zeitraum gezählt. An den Positionen 90° und 135° dauert es im echten Experiment Minuten bis zu einem einzigen Blitz.
Aber wir haben ja nicht so viel Zeit und daher darfst Du das abkürzen:
- Schalte Zeitraffer → × 10 oder × 100
- Die Blitze kommen jetzt entsprechend schneller
Der Zeitraffer verändert nichts an der Physik – er zeigt dir nur, was sich über eine viel längere Zeit angesammelt hätte
Du kannst dir die Auswertung etwas leichter machen: in späteren Experimenten wurde der ZnS-Schirm durch einen Fotofilm ersetzt, der den gesamten Kreisring abdeckte. So ein Film wurde eine Weile bestrahlt und dann chemisch entwickelt. Jeder Treffer hinterließ einen schwarzen Punkt.
- Detektor → Fotofilm umschalten
- Aufnahme starten drücken und warten (oder mit Zeitraffer beschleunigen)
- Nach Abschluss: Film entwickeln drücken
Der entwickelte Film zeigt dir die Verteilung aller Treffer auf einmal.
Wo sind die meisten Alphateilchen hingegangen? Und was bedeuten die wenigen, vereinzelten Punkte?
Was macht man mit dem Ergebnis? Nun: eigentlich geht es darum, nachzuvollziehen, welchen Weg die alpha-Teilchen in bzw. ab der Goldfolie eingeschlagen haben.
Die Forscher konnten die Flugbahnen der Alphateilchen nie direkt sehen – sie haben sie nur aus den Ergebnissen erschlossen.
Das kannst du auch so machen. Aber du darfst auch die Teilchenbahnen „einschalten“:
- schalte α-Teilchen → sichtbar
- und du erhälts einen „Animation der Teilchen“
Denke gerne mal nach: wie kommt man von den Blitzen auf dem Leuchtschirm oder den schwarzen Punkte auf dem Fotofilm auf die Teilchenbahnen? Wohin sind die meisten Teilchen geflogen und was passierte mit einzelnen anderen?
Was sagte Rutherford?
Weiteres
Geiger und Rutherford im Gespräch im Labor6
Rutherford hatte mit geringen Ablenkungen gerechnet – für das Atom Modell nach Thomson wäre das die erwartete Antwort gewesen.
Weiteres
Dann kam Geiger aufgeregt zu ihm. Was er berichtete, war eindeutig: Die meisten alpha-Teilchen flogen tatsächlich nahezu ungehindert durch die Folie. Aber einige wurden stark abgelenkt und …
we have been able to get some of the α-particles coming backwards …
… it is almost as incredible as if you had fired a 15-inch shell at a piece of tissue paper and it came back and hit you.7