Fallakte Ozeanversauerung
Jedes Team erhält seine eigene, persönliche Fallakte. Zudem sammeln wir alle Ergebnisse an einem gemeinsamen Bord – in digitaler oder analoger Form
Lasst uns den Fall Schritt für Schritt gemeinsam aufklären. Zwischendurch präsentieren und diskutieren wir immer im Plenum uns Zwischenergebnisse.
Weiteres
Das klären wir Schritt für Schritt.2
Schritt 1: Tatort erschließen, Hypothese formulieren
- Betrachten die gemeinsam im Team die Fallakte. Beschreiben Sie was Sie sehen bzw. zu erkennen glauben.
- Nutzen Sie M2 und ergänzen Sie erste Notizen auf dem Whiteboard zu Tatort, Opfer & Verdächtigem.
- Formulieren und notieren Sie auf Basis ihres Vorwissens eine experimentell prüfbare Vermutung zum Tathergang.
Nutzen Sie folgende Struktur: „Wir vermuten, dass CO2 im Meerwasser führt dazu, dass … weil wir bereits wissen, dass …“.
"Tatort, Opfer und Verdächtiger"
Ein "Freilandlabor" vor Italiens Küste
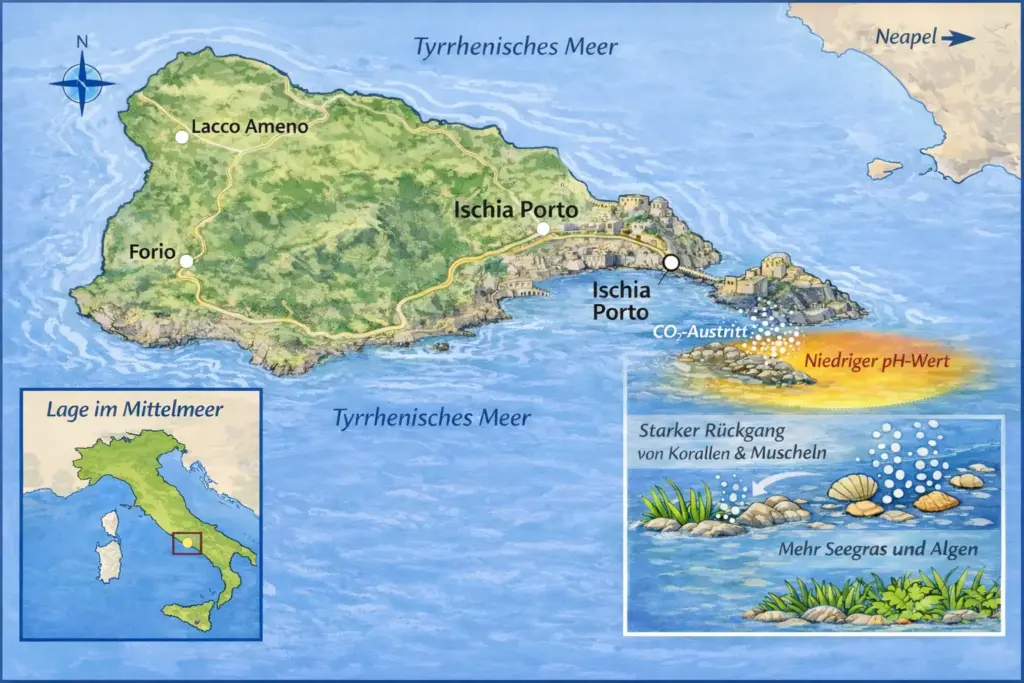
Vor der Insel Ischia treten sogenannte CO2-Vents auf. Dort gelangt Kohlendioxid aus vulkanisch aktiven Gesteinsschichten durch Spalten im Meeresboden ins Wasser. Dadurch sinkt der pH-Wert. In der Nähe der Vents ist dieser Effekt besonders stark, weiter entfernt nimmt er ab.
Dies macht den Ort spannend für Forschung: Ohne Labor kann man hier beobachten, wie unterschiedliche CO2-Konzentrationen Ökosysteme beeinflussen.34
Natürliche CO2-Quellen vor Ischia (nicht maßstabsgetreu) erzeugen einen pH-Gradienten im Meer und verändern das Ökosystem.5
So sähe es aus, wenn ein Tauchrobotor pH-Proben nähme
Was geschieht in diesem Freilandlabor?


Kalkhaltigen Organismen in natürlich versauertem Meerwasser.8
Zwei Befunde des Teams:
- Muscheln oder Korallen sind in der Nähe der CO2-Vents weniger verbreitet, während sich andere Arten wie Algen oder Seegras stärker ausbreiten.
- Gehäuse von Schnecken, die nahe der CO2-Vents leben, sind beschädigt. Vor allem ältere Schneckengehäuse zeigten deutliche Vertiefungen.
Schritt 2: Experiment als Spurensicherung, den Befund sichern
Ihre Vermutung steht auf dem Whiteboard. Jetzt holen Sie sich den Beweis.
- Lesen Sie die Durchführung von V1 und hier vor allem das Versuchsdesign.
- Führen Sie V1 durch. Fotografieren Sie Ihre Beobachtungen in den einzelnen Phasen und sichern sie Fotos digital.
- Formulieren Sie anschließend gemeinsam einen Befundsatz und schreiben Sie ihn als Beweisstück auf das Whiteboard:
„Wir haben beobachtet, dass … Das bedeutet für Ischia: … unsere Vermutung wird dadurch bestätigt / widerlegt / muss präzisiert werden, weil …“
Wir prüfen experimentell unsere Vermutung im Modellversuch
Versuchsdesign
Streng genommen sind es zwei Versuche:
- Da wir für die Untersuchung nur wenig Zeit haben, nutzen wir sehr fein verteilten Kalk. Die feine Verteilung erreichen wir, in dem wir den Kalk ganz frisch herstellen. Dazu geben wir Kohlenstoffdioxid in Calciumhydroxid-Lösung. Du kennst dies bereits als Kalkwasserprobe.
- Zu dem fein verteilten Kalk geben wir dann immer mehr Kohlenstoffdioxid.
Um den pH-Wert verfolgen zu können, geben wir von Beginn an Universalindikator hinzu.
Materialien
- Schutzbrille
- Spritze 12 mL
- Spritze 30 mL
- Dreiwegehahn
Chemikalien
-
Calciumhydroxid-Lösung
- sog. Kalkwasser
- Kohlenstoffdioxid
- Universalindikator-Lösung pH 1 - 13
Aufbau und Durchführung
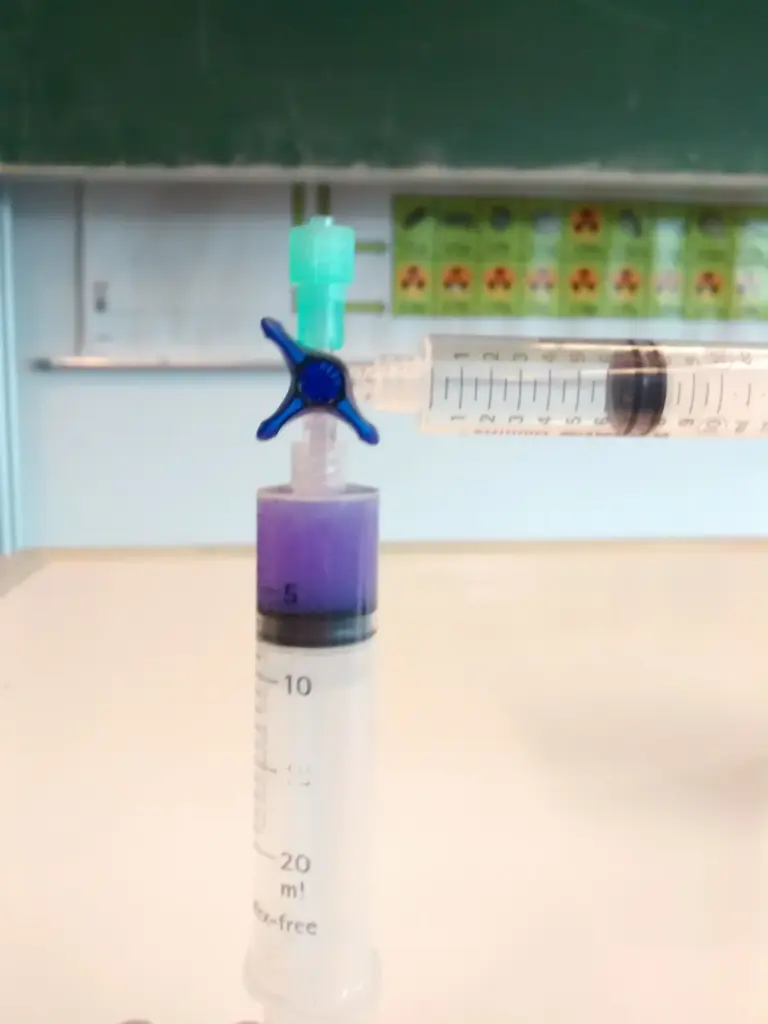
- Die Calciumhydroxid-Lösung wird mit wenigen Tropfen Universalindikator eingefärbt.
- 5 mL dieser Lösung werden in eine 30 mL Spritze aufgesaugt.
- Eine 12 mL Spritze wird mit Kohlenstoffdioxid gefüllt und über den Dreiwegehahn mit der großen Spritze verbunden.
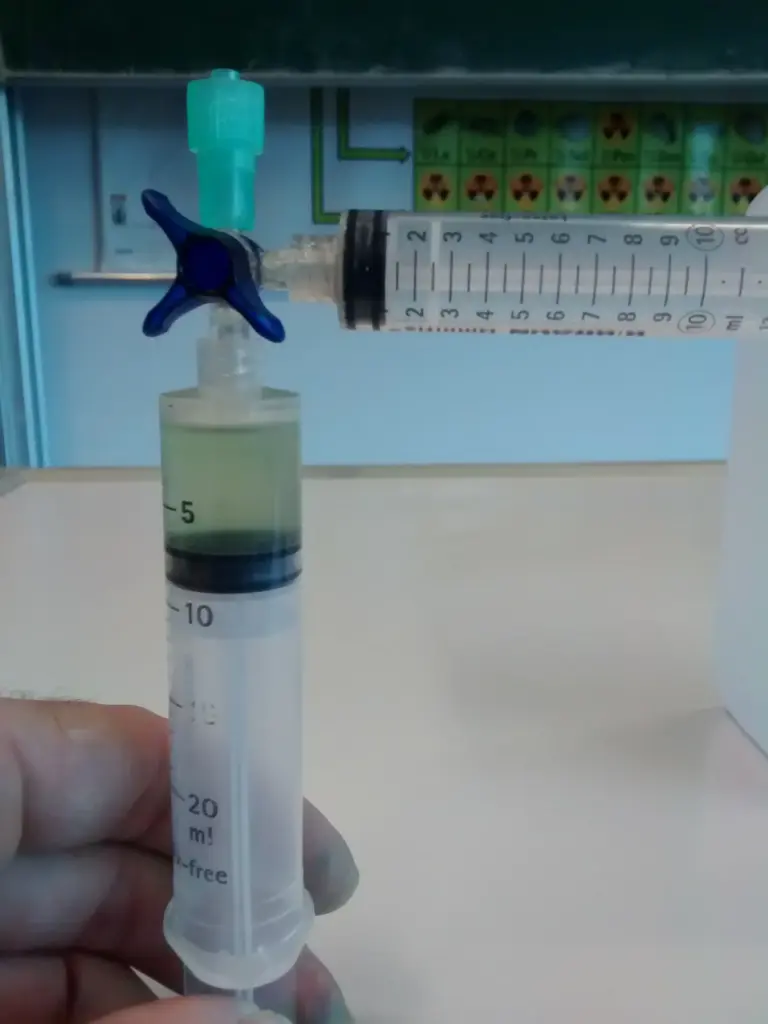
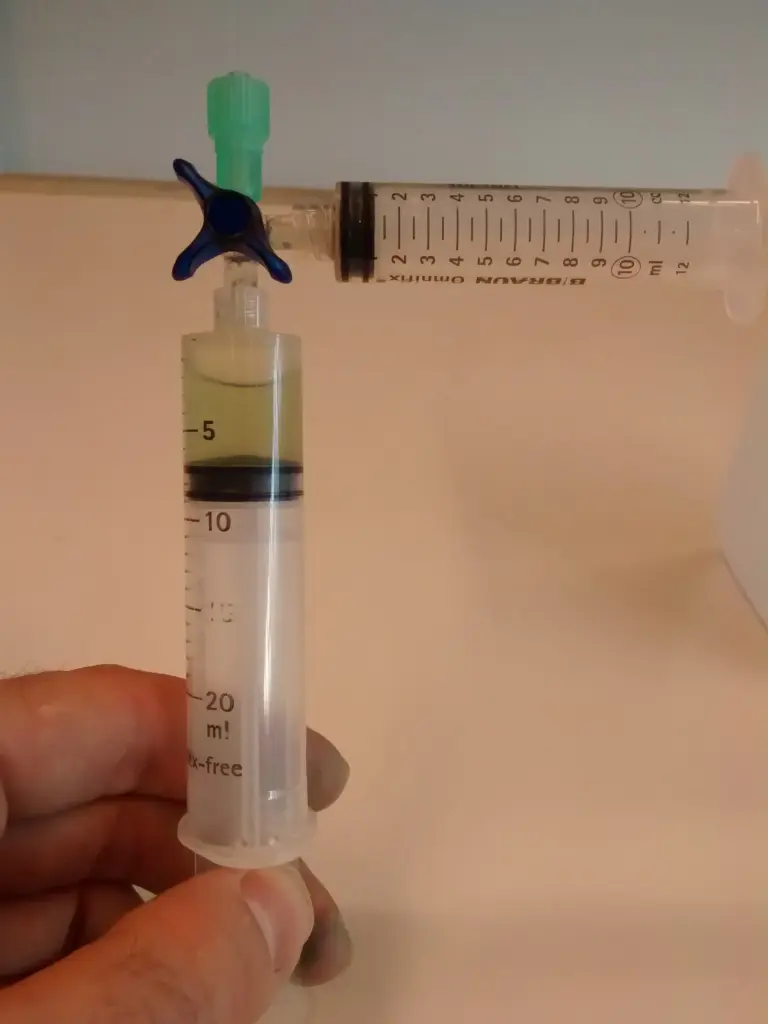
- Kohlenstoffdioxid wird in 2 mL Schritten zur Lösung hinzugefügt. Der Hahn wird nach jeder Zugabe geschlossen, das System vorsichtig geschüttelt und beobachtet.
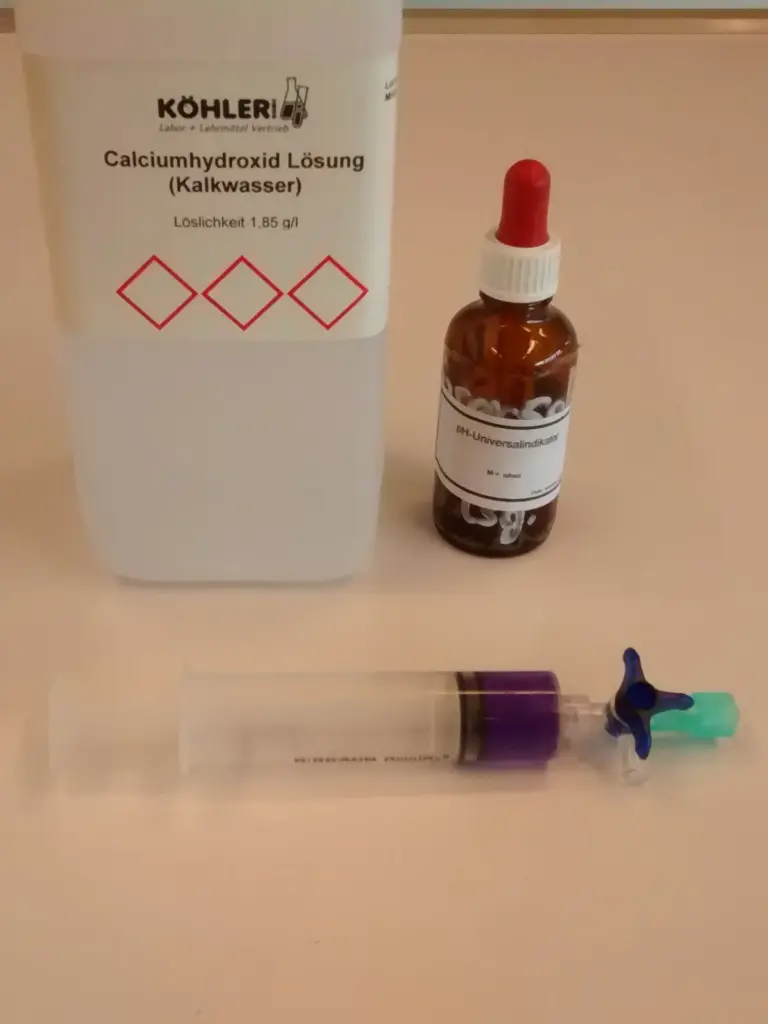
Aufbau zu Beginn1
Raum für Beobachtungen
Erstelle mehrere Fotos und notiere dazu, was du beobachten konntest.
Entsorgen und Aufräumen
-
Alle verunreinigten Labormaterialien spülen.
-
Alle Materialien an ihren Ursprungsort zurückstellen.
Schritt 3 – Den Tathergang chemisch erläutern
Ihre Spurensicherung hat gezeigt, dass die Zugabe von CO2 etwas verändert. Jetzt müssen Sie dies erläutern. Arbeiten Sie sich durch die drei Reiter von M2.
- Reiter „Kalk“: Beschreiben Sie den Unterschied zwischen Calciumcarbonat und Calciumhydrogencarbonat hinsichtlich ihrer Löslichkeit. Notieren Sie die Reaktionsgleichung zum Gleichgewicht zwischen beiden Stoffen. Wenden Sie darauf das Prinzip von Le Chatelier an: Was passiert mit diesem Gleichgewicht, wenn die CO2-Konzentration im Meerwasser steigt?
- Reiter „Kohlenstoffdioxid – Hydrogencarbonat – Carbonat“ Erklären Sie sich gegenseitig, wie aus gelöstem CO2 schrittweise Hydrogencarbonat-Ionen und Carbonat-Ionen entstehen. Diskutieren Sie, warum wir in Unkenntnis der Gleichgewichtskonstanten nichts über das Verhältnis von Carbonat zu Hydrogencarbonat sagen können.
- Reiter „Verhältnis der Konzentration nach pH-Wert“
Lesen Sie das Diagramm aus. Erklären Sie sich die Kurvenverläufe mit Hilfe der Reaktionsgleichungen im 2. Reiter und Le Chatelier. Leiten Sie ab: Was bedeutet ein sinkender pH-Wert für die Verfügbarkeit von Carbonat-Ionen – und damit für kalkbildende Lebewesen? - Tathergang formulieren: Fassen Sie die Erkenntnisse aus den Aufgaben 1–3 zusammen. Erläutern Sie den Tathergang in einer zusammenhängenden Argumentation: Warum führt steigendes CO₂ dazu, dass kalkbildenden Lebewesen die Grundlage für den Aufbau ihrer Schalen entzogen wird? Nutzen Sie Reaktionsgleichungen und das Prinzip von Le Chatelier. Tragen Sie den Tathergang als Beweisstück auf Ihr Whiteboard ein und stellen Sie Ihren Tathergang anschließend im Plenum vor.
Das Carbonat-Hydrogencarbonat-Gleichgewicht
Weiteres
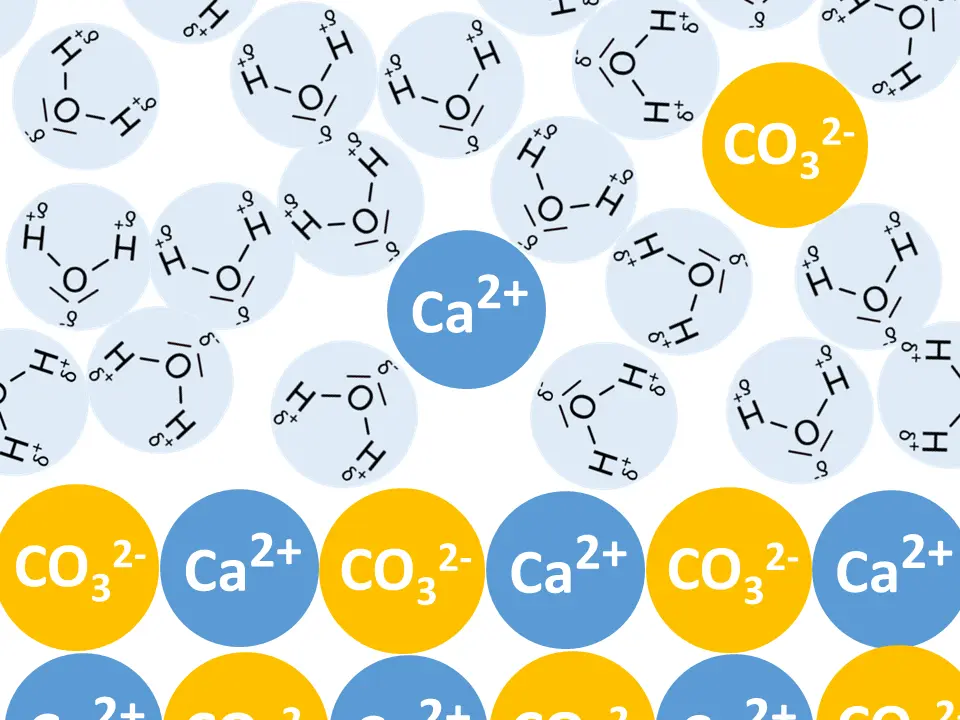
Muschelgehäuse und Korallenskelette bestehen aus Kalk (Calciumcarbonat, Formel: CaCO3).
Calciumcarbonat ist sehr schlecht wasserlöslich. Auch unter Wasser liegt er überwiegend als Feststoff in der kristallinen Form vor.
Schematische Darstellung von Kalk unter Wasser9
Weiteres
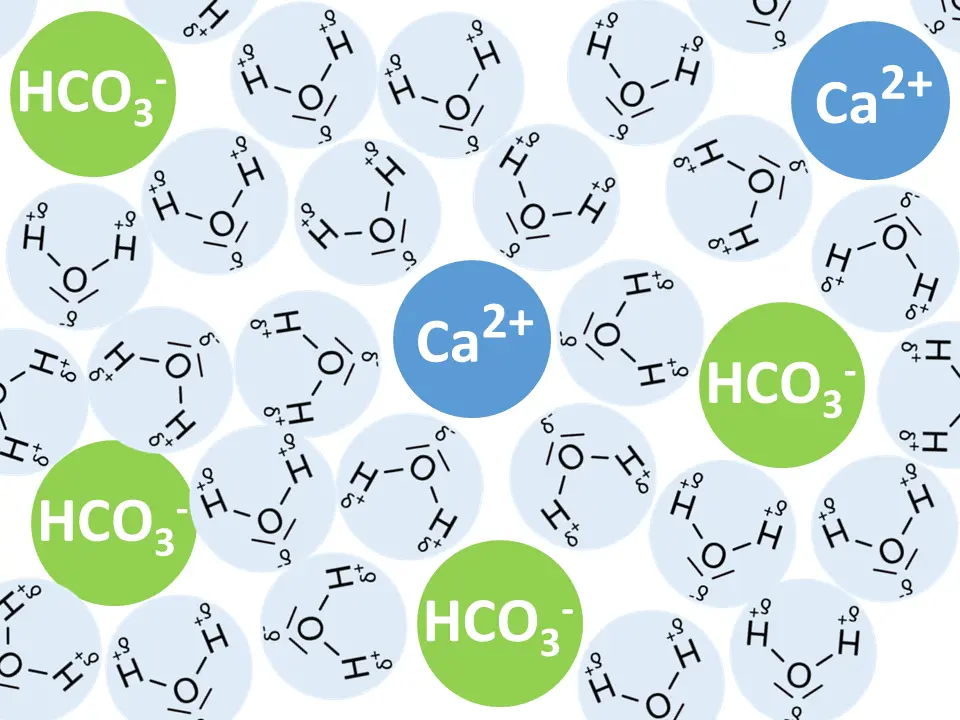
Calciumhydrogencarbonat ist so gut wasserlöslich, dass es nur in gelöster Form vorliegt.
Schematische Darstellung der Lösung9
Weiteres
Calciumhydrogencarbonat und Calciumcarbonat stehen in einem Gleichgewicht miteinander. Vereinfacht können wir sagen:
Ob nun also vermehrt Calciumhydrogencarbonat oder Calciumcarbonat vorliegen, hängt davon ab, ob die Lösung reich an an Carbonat-Ionen ist oder an Hydrogencarbonat-Ionen. Und das hängt wiederum von der Kohlenstoffdioxidkonzentration ab.
Weiteres
Schauen wir uns die bereits bekannten Gleichgewichte rund um das Kohlenstoffdioxid noch einmal genauer an. Sie zeigen, wie die Ionen entstehen:
Weiteres
Überlegen wir zuerst einmal, was passiert, wenn die Lösung stark alkalisch ist und dann der pH-Wert immer kleiner wird.
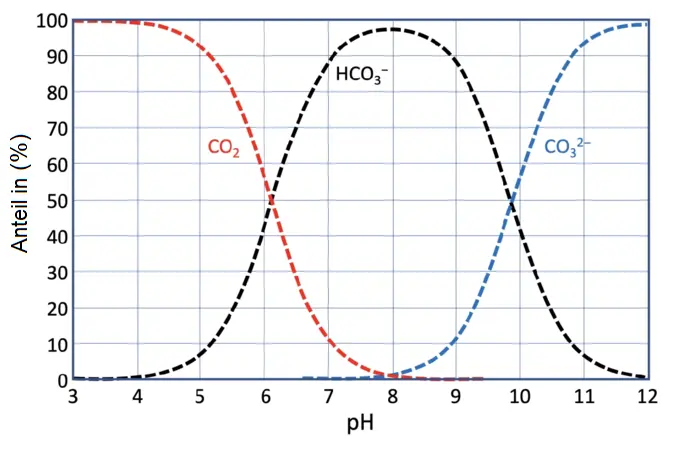
Schauen wir uns dann folgendes Diagramm an. Es zeigt exakt, wieviel Kohlenstoffdioxid, Hydrogencarbonat oder Carbonat bei welchem pH-Wert vorliegen:
Der Anteil an Kohlenstoffdioxid-Hydrogencarbonat-Carbonat im Meerwasser in Abhängigkeit vom pH-Wert.10
Anregungen
Das Diagramm zeigt: bei pH-Werten kleiner als 4 liegt fast nur Kohlenstoffdioxid vor. Bei pH-Werten um die 8,2, also den Werten der vorindustriellen Zeit im Meerwasser, fast ausschließlich Hydrogencarbonat und bei deutlich höheren pH-Werten fast ausschließlich Carbonat.
Schritt 4 – Vom Tatort zur globalen Dimension
Ischia als Untersuchungsort war kein Zufall. Die Forschenden haben diesen Ort bewusst gewählt – weil der natürliche pH-Gradient dort abbildet, was sich global ankündigt.
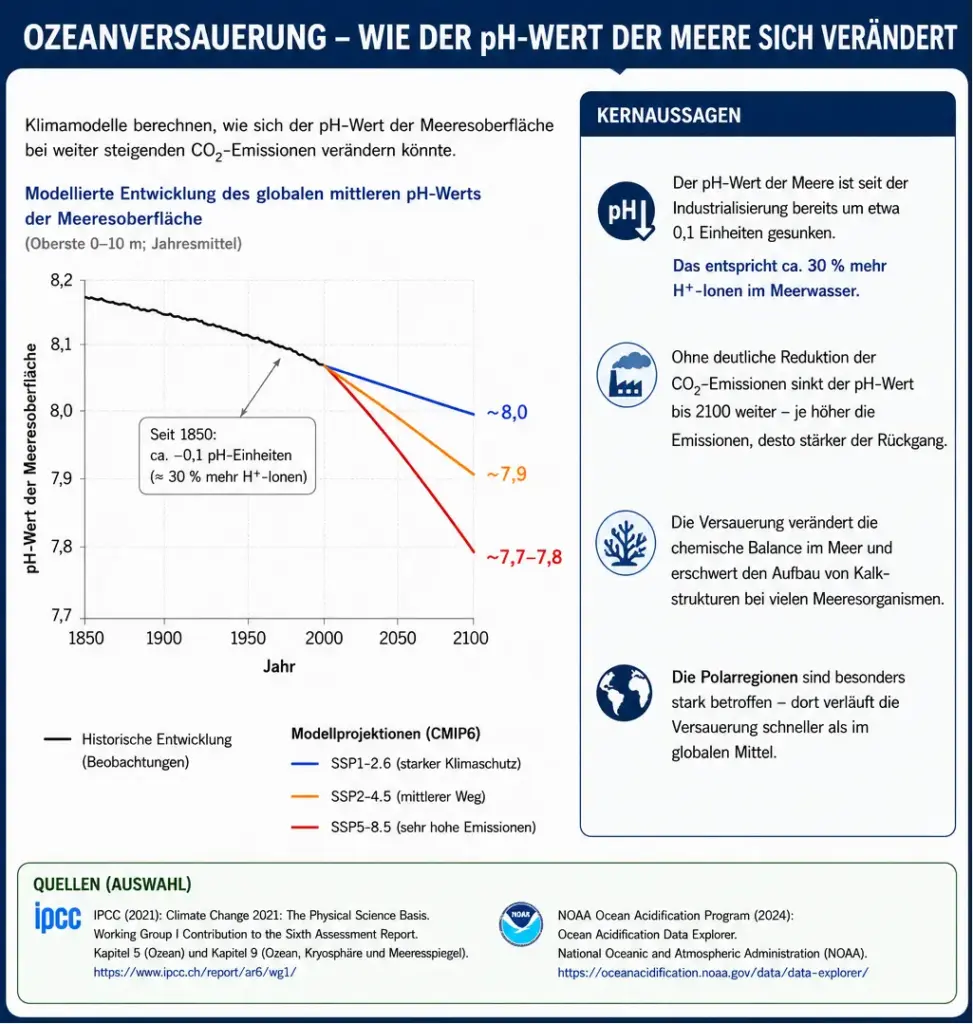
- Lesen Sie M4 und werten Sie das Diagramm zur Entwicklung des globalen pH-Werts aus. Beschreiben Sie, wie sich der pH-Wert der Meere seit 1850 verändert hat und welche Entwicklung die drei Szenarien bis 2100 projizieren.
- Erläutern Sie die Aussage: „Kalkbildende Lebewesen bekommen selbst im günstigsten Szenario Probleme“.
- Nehmen Sie Stellung: Stellt die Ozeanversauerung aus ihrer Sicht einen problematischen menschlichen Eingriff in Stoffkreisläufe dar? Begründen Sie ihre Aussage und tragen Sie sie in die gemeinsame Planetare-Grenzen-Übersicht ein.
Ergebnisse der Messungen und Prognosen weltweit
Beobachtungesergebnisse von Hall Spencer und weltweit
Allgemein konnten Hall Spencer und sein Team beobachten, dass kalkbildende Organismen wie Schnecken, aber auch Seeigel und Korallen in derartigen Gebieten kaum existieren.
- Durch die Schwächung der Kalkgehäuse werden Schnecken anfälliger für Raubfeinde.
- Junge Schnecken entwickeln sich kaum in Regionen mit pH-Werten von pH ≤ 7,4.
Die Forschungsergebnisse betonen, dass eine langfristige Absenkung des pH-Werts durch die heutige CO2-Erhöhung ähnliche Effekte global hervorruft. Zusammen mit der zunehmenden Erwärmung sind z. B. Korallen damit auf zwei Wegen gleichzeitig gefährdet.
Warum diese Ergebnisse wichtig sind: Schnecken sind primäre Nahrung für viele Meeresbewohner. Ihr Verlust stört die Nahrungskette. Der Verlust von Korallenriffen mit ihrer hohen Artenvielfalt ist eine noch gravierendere Folge der Ozeanversauerung!
Weiteres
Vereinfachte schematische Darstellung auf Grundlage publizierter Beobachtungs- und Modellierungsdaten.11
Glückwunsch: Sie haben den Tathergang aufgeklärt: Anstieg der CO2-Konzentration bedingt eine Erniedrigung der Carbonat-Konzentration im Meerwasser – Kalkbildung wird erschwert. Und jeder weiß ja auch: Kalk löst sich in Säure auf.
Aber das Meerwasser ist heute noch alkalisch. Warum zeigen Schnecken, Korallen und Seeigel trotzdem schon jetzt Probleme?
Wer dieser Frage nachgehen möchte, findet hier eine Antwort.
Schritt 5 - freiwillig - warum gibt es bereits im leicht alkalischen Milieu Probleme
- Lesen Sie den Text und betrachten Sie die Abbildung oder schauen Sie sich das Video an.
- Erläutern Sie in eigenen Worten, warum kalkbildende Organismen bereits im schwach alkalischen Milieu Schwierigkeiten haben, Kalkskelette aufzubauen – obwohl Kalk unter diesen Bedingungen nicht gelöst wird.
- Ergänzen Sie gerne noch die ein oder andere Erkenntnis als letztes Beweisstück in Ihrer Fallakte.
Komplexere Zusammenhänge - für Interessierte
Weiteres
Noch ist das Meerwasser nicht sauer. Warum haben Schnecken, Korallen, Algen aber bereits jetzt Probleme, Kalk zu produzieren? Dazu muss man verstehen, dass all diese Lebewesen an die lange Zeit vorherrschende Situation im Meer angepasst waren.
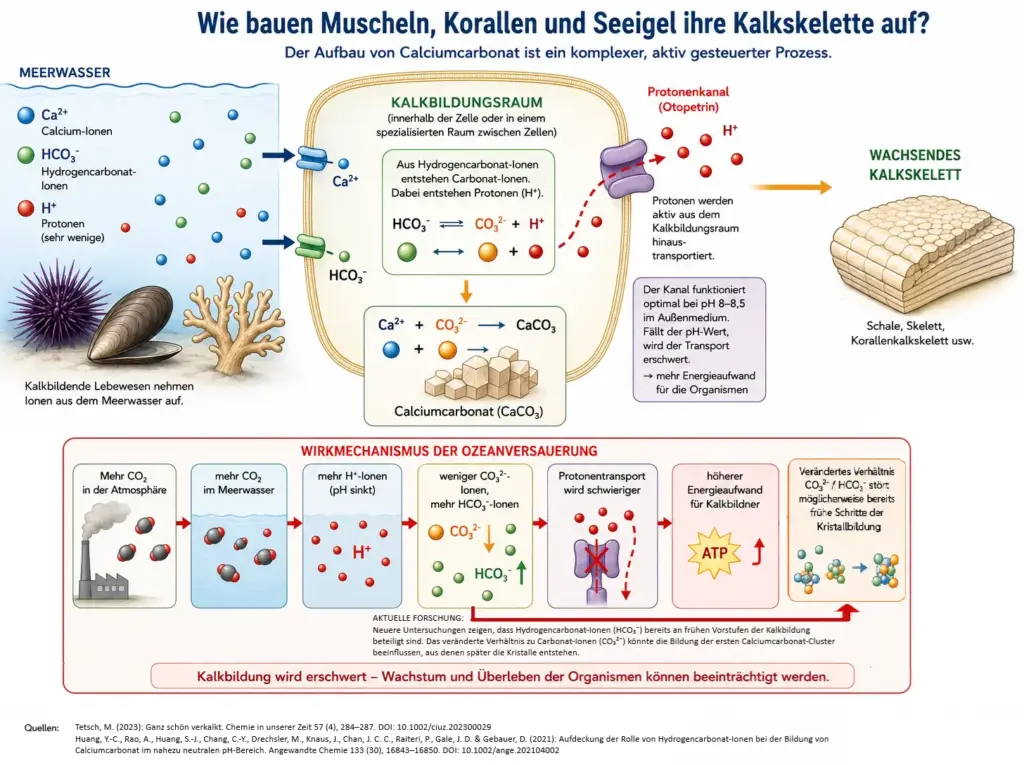
Kalkbildende Lebewesen bauen ihre Schalen und Skelette nicht durch passives Ausfällen von Calciumcarbonat auf. Dieser Prozess ist aktiv gesteuert und erfordert Energie.
Im Inneren spezialisierter Zellen oder Zellräume (Kalkbildungsraum) entstehen aus Hydrogencarbonat-Ionen (HCO3–) zunächst Carbonat-Ionen (CO32-). Dabei entstehen Protonen (H+), die aktiv aus dem Kalkbildungsraum herausgeschleust werden müssen – durch einen Protonenkanal namens Otopetrin. Dieser Kanal funktioniert jedoch nur unter bestimmten pH-Bedingungen optimal: Sinkt der pH-Wert im Außenmedium unter etwa 7,5, erliegt der Fluss nahezu vollständig. Schon bei heute messbaren pH-Werten ist der Mechanismus beeinträchtigt.12
Neuere Untersuchungen zeigen zudem, dass Hydrogencarbonat-Ionen an den allerersten Schritten der Kalkbildung beteiligt sind: Sie beeinflussen die Bildung winziger Calciumcarbonat-Cluster, aus denen später die eigentlichen Kristalle entstehen. Dazu wird ein bestimmtes Verhältnis benötigt. Ob und wie eine Verschiebung die Kristallbildung beeinflusst, ist Gegenstand aktueller Forschung.13
Weiteres
Vereinfachte schematische Darstellung der Biomineralisation und möglicher Auswirkungen der Ozeanversauerung auf kalkbildende Organismen.14
Weiteres
Dr. Sebastian Rokitta vom Alfred-Wegener-Institut erklärt noch andere Auswirkungen der zunehmenden Versauerung des Meerwassers anhand von Kalkalgen: