Das Prinzip von Le Chatelier
Weiteres
„Wird auf ein System, das sich im chemischen Gleichgewicht befindet, ein äußerer Zwang ausgeübt, stellt sich ein verändertes Gleichgewichts so ein, dass die Wirkung des Zwanges minimal wird.“
Weiteres
Im Zusammenhang mit dem Prinzip von Le Chatelier wird oft davon gesprochen, dass sich „das Gleichgewicht auf die Produktseite oder die Eduktseite verschiebt“. Das klingt komisch.
Gemeint ist eigentlich, dass nach der Störung des ursprünglichen Gleichgewichts kurzfristig die Reaktionsrate entweder zur vermehrten Bildung von Produkten oder Edukten überwiegt.
Aufgaben
- Betrachten Sie das Video und erklären Sie die prinzipielle Aussage, die in dem Prinzip von Le Chatelier zum Ausdruck kommt, unter Verwendung der Begriffe Störung und Neueinstellung eines Gleichgewichts.
- Einzelarbeit: Kopieren Sie aus den Vorlagen die tabellarische Übersicht und vervollständigen Sie diese mit Hilfe von M2.
- Partnerarbeit: Kopieren Sie aus den Vorlagen den Beginn der Concept-Map und vervollständigen Sie die Map.
Vorlagen

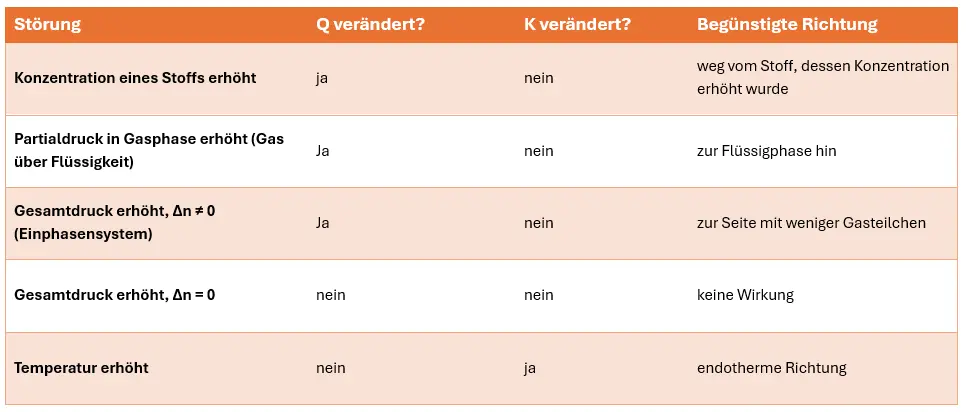
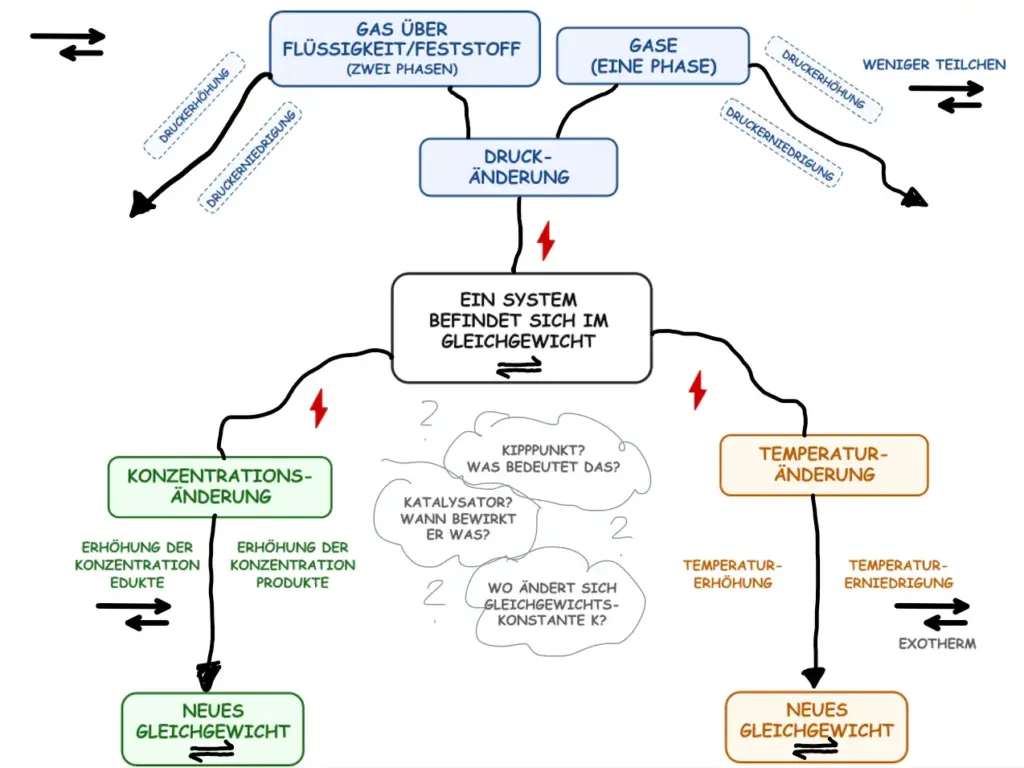
Das Prinzip im Überblick: Konzentration, Druck und Temperatur
Die Gleichgewichtskonstante Kc
Stellen wir uns eine beliebige Gleichgewichtsreaktion vor:
KC beschreibt nun das Gleichgewicht über die Stoffmengenkonzentrationen der beteiligten Stoffe in mol/L.
Produkte stehen im Zähler, Edukte im Nenner – jeweils mit dem stöchiometrischen Koeffizienten als Exponent. Reine Feststoffe und Lösungsmittel tauchen nicht auf, weil ihre Konzentration konstant bleibt.
Drei Arten von äußerem Zwang – drei unterschiedliche Wirkungen
Wir haben drei Faktoren kennengelernt, die ein Gleichgewicht stören können. Sie wirken jedoch grundlegend unterschiedlich – und das zeigt sich besonders darin, was mit der Gleichgewichtskonstante K passiert.
Konzentration
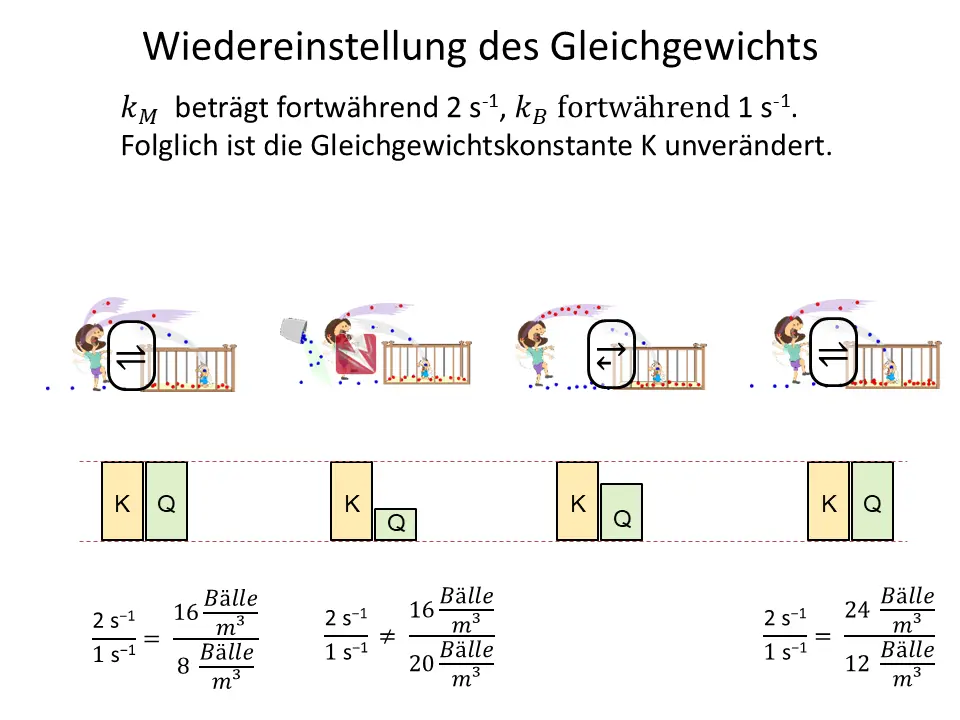
Erhöht oder erniedrigt man die Konzentration eines beteiligten Stoffs, weicht der Massenwirkungsquotient Q vorübergehend von K ab. Die Reaktion läuft verstärkt in die Richtung, die Q wieder an K angleicht – bis sich ein neues Gleichgewicht mit veränderten Konzentrationen eingestellt hat.
Analogie zur Konzentrationsänderung1
Druck
„Druck erhöhen“ kann in zwei verschiedenen Systemtypen auftreten, die sich unterscheiden.
Zweiphasensystem: Gas über einer Flüssigkeit
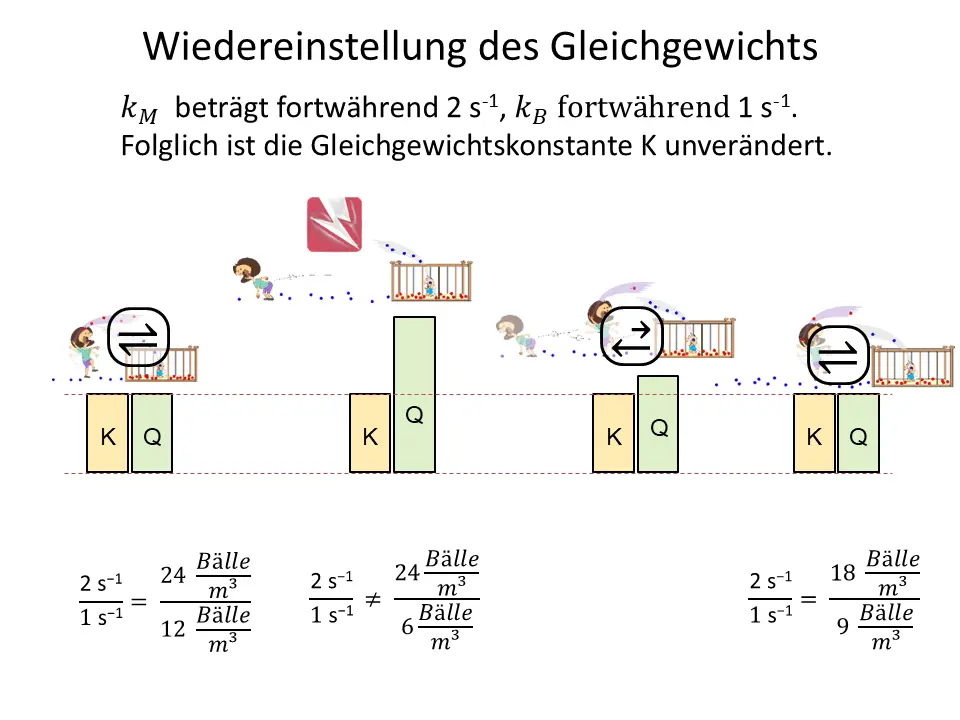
Erhöht man den Partialdruck eines Gases zum Beispiel durch Einpressen von CO2 in der Gasphase über dem Wasser, so steigt die Konzentration des gelösten CO2 in der wässrigen Phase an, bis sich ein neues Gleichgewicht eingestellt hat. Verringert man den Druck, gilt das Umgekehrte2
Konzeptuell handelt es sich bei der Druckveränderung in einem Zweiphasensystem eigentlich um eine Konzentrationsveränderung in der Gasphase.
Analogie zur Druckänderung 2 Phasen1
Einphasiges System: alle Reaktionspartner sind gasförmig
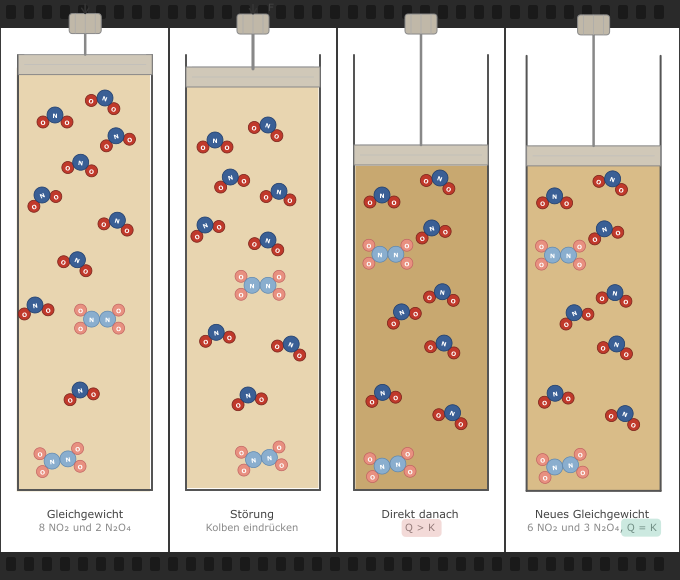
Anders verhält es sich, wenn alle Reaktionspartner gasförmig sind. Eine Druckveränderung durch Volumenänderung des Behälters beeinflusst die Gleichgewichtslage dann, wenn auf Edukt- und Produktseite unterschiedlich viele Gasmoleküle beteiligt sind. Als eindrucksvolles Beispiel – auch weil es sichtbar ist – dient das Stickstoffdioxid-Gleichgewicht:
NO2 ist rotbraun, N2O4 ist nahezu farblos. Das Gleichgewicht lässt sich daher direkt beobachten: Eine Druckerhöhung (Volumenverkleinerung) erhöht die Konzentration aller Gase gleichzeitig. Das Gemisch wird zunächst dunkler. Das System stellt sich dann neu ein und die Gasmischung hellt sich wieder auf.
Modell zur Druckänderung in 1 Phase1
Temperatur
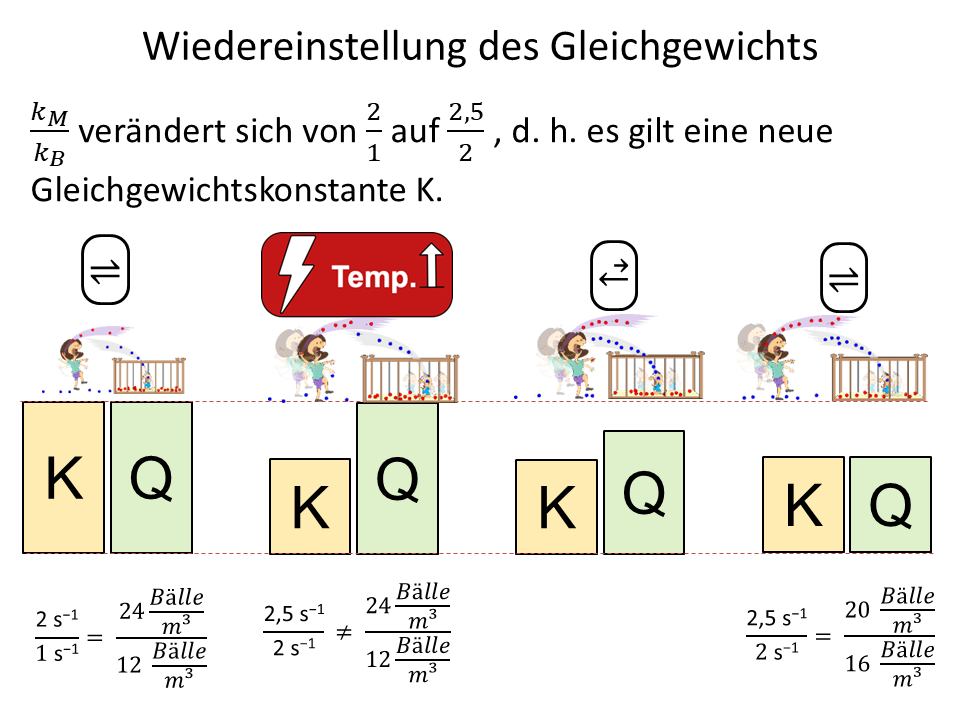
Die Temperatur ist der einzige Faktor, der K selbst verändert. Das ist der entscheidende Unterschied zu Konzentration und Druck.
Analogie zur Temperaturveränderung1
Bei einer Temperaturerhöhung wird stets die endotherme Reaktionsrichtung begünstigt, bei einer Temperaturerniedrigung die exotherme. Das neu eingestellte Gleichgewicht besitzt einen anderen K-Wert als das ursprüngliche.
Ob eine Reaktionsrichtung endo- oder exotherm ist, lässt sich an der Reaktionsenthalpie ΔH ablesen:
- ΔH < 0: die Hinreaktion ist exotherm (gibt Energie ab)
- ΔH > 0: die Hinreaktion ist endotherm (nimmt Energie auf)
Die Lösung von CO2 in Wasser ist zum Beispiel exotherm.
Eine Temperaturerhöhung begünstigt die Rückreaktion – CO2 verlässt die Lösung.
Merke: Eine Tabelle mit K-Werten ist deshalb immer mit einer Temperaturangabe verbunden. Der K-Wert einer Reaktion bei 25 °C ist ein anderer als bei 50 °C.
Weiteres
Haben Katalysatoren eigentlich einen Einfluss auf die Gleichgewichtslage?
Nein. Sie beschleunigen Hin- und Rückreaktion gleichermaßen. Bei Zugabe eines Katalysator stellt sich also kein neues Gleichgewicht ein, sondern das Gleichgewicht stelle sich einfach schneller ein!